GENERALITES SUR LES SOLUTIONS AQUEUSES
DEFINITIONS
Solution
. Une solution peut être définie comme un mélange homogène
dont les constituants sont divisés et dispersés l'un dans l'autre au niveau
moléculaire. · Une solution est toujours constituée : ·
d'un ou plusieurs solutés:
Les
solutés peuvent être : -un
gaz: CO2 dans les boissons gazeuses, O2, HCl… -un solide : sel.
La masse m est exprimée en gramme(g) Le volume V souvent exprimé en litre(l) . La concentration Cm en gramme par litre(g/l)
On appelle concentration molaire d’une solution la quantité (en moles) de
soluté dissout dans un litre de solution. Soit
n le nombre de moles de soluté introduit dans l’eau pour obtenir un volume V de
solution, la concentration de la solution obtenue est: n: la
quantité de matière de A en solution en mole (mol) V: volume de la
solution en litre(l). C: concentration
molaire en môle par litre (mol/l)
Déterminer la concentration d’une eau salée obtenue en dissolvant 0,6g de
chlorure de sodium dans l’eau et en complétant le volume a 200 cm3. On
donne les masses molaires atomiques:Na:23; Cl:35,5 MNaCl=23+35,5=58.5
g/mol V=0,2 l n=0.6/58,5=0,01mol C=
n/V=0,01/0,2=0,05 mol.l-1
Remarque: Les
chimistes utilisent parfois les adjectifs molaire, decimolaire,
centimolaire…pour caractériser des solutions de concentrations 1mol.l-1,0,1
mol.l-1,0,01mol.l-1…
Concentration d’une espèce en solution
V: volume de la
solution en litre(l). [A]: concentration molaire
en môle par litre (mol/l)
NaCl
→ Na+ +Cl-
1mol 1mol 1mol
En divisant partout par
V, on obtient [Na+]=[Cl-]=[NaCl] or
Donc [Na+]=[Cl-]= 0,1
Dans toute solution aqueuse, le produit des concentrations molaires des ions H3O+
et HO- à l’état d’équilibre et à une température donnée, est une
constante appelée constante d’équilibre d’autoprotolyse de l’eau. Cette
constante notéeKe. Ke est aussi appelée produit
ionique de l’eau.
Ke=[H3O+][HO-]
Ke
est un nombre sans dimension qui dépend de la température. A
25°C, on a Ke =10-7.10-7=10-14 Le
produit ionique Ke étant une grandeur très faible, on lui associe souvent une
autre grandeur pKe telle que:
pKe = -logKe
Ainsi
à 25°C, pour l’eau, on a Ke=10-14 d’où
pKe=-log10-14=
14
Toute solution aqueuse contient des ions H3O+ . Les
propriétés acides ou basiques d’une telle solution dépendent de la
concentration molaire en ions H3O+. Cette concentration
généralement faible, s’exprime en puissances négatives de 10.
: Le pH (potentiel hydrogène)
d'un solvant (constituant majoritaire): lorsque le solvant est l'eau la
solution est dite aqueuse.
-un liquide : éthanol, …
La concentration massique Cm
C'est le rapport de la masse d’un composé X contenu
dans un certain volume de solution divisée par ce volume de cette solution.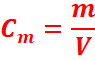
Exemple
On dissout 5 g de sulfate de cuivre (CuSO4) dans 400 ml d’eau. Quelle
est alors la concentration massique du sulfate de cuivre ?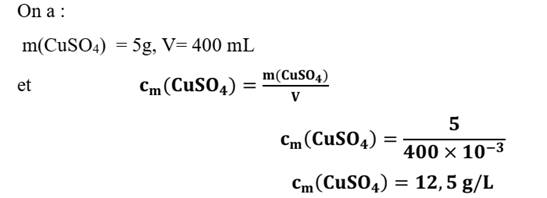
Concentration molaire d’une solution
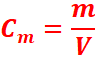
La concentration molaire d’une espèce chimique A en
solution notée [A] est la quantité de matière de cette espèce présente dans un
litre de solution.
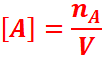
nA: la quantité de matière de A en solution en mole
(mol)
Exemple: On dissout 0,585 g de
NaCl dans 100 ml d’eau. Calculons les concentrations molaires de chaque espèce
en solution.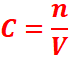
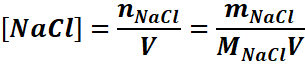
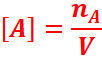
![]()
PRODUIT
IONIQUE DE L’EAU
DEFINITION ET
MESURE DU PH
Définition
Par la formule:
pH =-log[H3O+] =10-pH <=>[H3O+]=10-pH
[H3O+] est exprimée en mol.l-1
Mesure du pH:
On peut utiliser:
-utiliser un pH-mètre
-utiliser le papier pH
-utiliser les indicateurs colorés
pH des solutions aqueuses
Toutes les solutions aqueuses (dans
l’eau) sont neutres, acides ou basiques.
a. Une solution neutre est obtenue quand la concentration des ions hydronium
est égale à la concentration d’ions hydroxyde :
[H3O+] = [OH-]
b. Une solution acide est obtenue quand la concentration des ions hydronium est
supérieure la concentration d’ions hydroxyde :
[H3O+] > [OH-]
c. Une solution basique est obtenue quand la concentration des ions hydronium
est inférieure la concentration d’ions hydroxyde :
[H3O+] < [OH-]
. La plupart des concentrations d’ions hydronium sont très faibles
(c.-à-d. 4 × 10-8 mol/L ou 0,000 000 04 mol/L) d’où la proposition de potentiel
d’hydrogène, l’échelle de pH par Soeren Sorensen.
|
Le pH est une grandeur qui permet de classer les
solutions acides, basiques ou neutres. Une solution aqueuse est :
pH>7 <= >[H3O+]<[HO-]=>pH>1/2pKe
-Neutre si son pH = 7: pH=7 <=>[H3O+]=[HO-]=>pH=1/2pKe -Basique si son pH>7: pH<7 <= >[H3O+]<[HO-]=>pH>1/2pKe |
Exemple:
Une solution de pH= 3 est une solution acide dont la concentration
molaire en ions H3O+ est [H3O+]= 10-3
mol.L-1
Remarques :
Plus le pH est élevé, plus la concentration en ions H3O+
est faible et plus la solution est basique
Plus pH est faible, plus la concentration en ions H3O+
est élevée et plus la solution est acide
ÉQUATIONS DE CONSERVATION
Neutralité électrique d’une solution
Une solution aqueuse ionique a une charge électrique totale nulle: il y a autant de charges positives que de charges négatives.
Par définition, lorsqu’une solution contient des ions Aa+, Bb+,….,Xx-,Yy- …l’équation qui traduit son électroneutralité s’écrit:
a[Aa+]+ b[Bb+]+…..= x[Xx+]+y[Yy+]…
Exemple:
Soit l’équation:
Al2(SO4)3 → 2Al3+ + 3SO42-
La neutralité permet d’écrire:
3[Al3+]=2[SO42-]
·Conservation de la matière
C’est l’équation de la conservation d’un élément ou groupe d’éléments au cours d’une réaction chimique. Elle varie suivant que la réaction est totale ou limitée.
Exemple: Soit l’équation:
NaCl → Na+ +Cl-
La concentration de la solution en NaCl est:
C0=n0(NaCl)/V=n0(Na)=n0(Cl-)/V
Equation de conservation de la matière (ECM):
C0=[Na+] = [Cl-]
EXERCICES
EXERCICE I:
On dissout dans l’eau 8 g du sulfate de cuivre de formule CuSO4 dans 100 ml d’eau.
1-Ecrire l’équation de dissolution du sulfate de cuivre dans l’eau.
2-Calculer la masse molaire du sulfate de cuivre.
3-Calculer la concentration massique du sulfate de cuivre dans cette solution.
4-Calculer la concentration molaire du sulfate de cuivre dans cette solution.
On donne: Cu:64; O:16; S:32
EXERCICE II:
On dissout 0,01 mol de chlorure de calcium CaCl2 dans 250 cm3 d’eau.
1-Determiner la masse de chlorure de calcium nécessaire.
2-La solution précédente est complétée a 500 cm3 avec de l’eau; on obtient ainsi une solution de pH=7 à 25 °C.
a-Calculer les concentrations molaires des ions ca2+ et Cl-.
b-Vérifier la neutralité électrique de la solution et exprimer par une relation les concentrations molaires [ca2+] et [Cl-].
EXERCICEIII:
On dissout une masse m=20g de sulfate aluminium Al2(SO4)3 dans 500 cm3 d’eau.
1-Calculer la concentration molaire de chaque ion en solution.
2- Vérifier la neutralité électrique de la solution et exprimer par une relation les concentrations molaires [Al3+] et [SO42-].
On donne les masses molaires atomiques en g.mol-1: Al=27. S=32.1 O=16
EXERCICE IV:
1.Le pH du café contenu dans une tasse est de 5,8 à 25 C. Calculer les concentrations molaires des ions H3O+ et OH-.
2.A 25°C, un jus de tomate et une eau de lessive ont pour pH 4,1 et 11,2 respectivement. Pour chacune de ces solutions, calculer les concentrations molaires en ions H3O+ et OH- .
3.Classer, par ordre croissant de leur acidité, les solutions caractérisées à 25 C par:
a-pH=2,8
b-[HO-]=1,5=1,5.10-3 mol/l
c-[H3O+]=[HO-]
d-[H3O+]=0,045 mol/l
e-pH=8,3
EXERCICE V:
1.On dissout un volume V de chlorure d’hydrogène de concentration 1 mol/l dans l’eau pure, pour obtenir 100 cm3 d’une solution chlorhydrique de concentration 5.10-2 mol/l. Calculer le volume V.
2.On dissout 4g de cristaux d’hydroxyde de sodium dans 1l d’eau pure.
a-Calculer la concentration de la solution obtenue.
b-Quel volume d’eau pure doit-on ajouter à 5 ml de cette solution pour obtenir une solution de pH =11 à 25 C?
3-Une solution aqueuse de chlorure d’hydrogène, de concentration C=1.0.10-2mol/l, a un pH=2 à 25. °C
a-Calculer les concentrations molaires en ions H3O+ et OH- .
b-Quel volume de chlorure d’hydrogène HCl a-t-il fallu dissoudre dans 500 ml d’eau pour obtenir cette solution, sachant que dans les conditions de l’expérience, le volume molaire est 25 l/mol?
c-Comparer C et [H3O+].La solution contient-elle des molécules HCl?
EXERCICE VI:
A 80°C , la valeur de pKe est 12,6.
1-Determiner la valeur du produit ionique de l’eau à 80 °C.
2-En déduire le pH de l’eau pure a cette température.
3-A la même température, une solution aqueuse a un pH=4,3. Calculer la concentration molaire des ions HO-.
EXERCICE VII:
La réaction entre l’ethanamine (Cb=8,84.10-2 mol.l-1, Vb=6 ml) et les ions H3O+ de la solution d’acide chlorhydrique( Ca=10-1 mol.l-1,Va=10 ml) a pour équation:
C2H5NH2 + H3O+ → C2H5NH3+ + H2O
La solution obtenue a pour pH la valeur 1,5.
1.Identifier les espèces chimiques en solution
2.Ecrire l’équation de neutralité électrique. En déduire la concentration des ions C2H5NH3+
3.Ecrire l’équation de conservation de la matière pour l’élément azote. En déduire la concentration C2H5NH2
CORRIGES
Avez-vous un exercice à proposer au Forum?Cliquez-ici
CORRIGES
Merci de votre
visite
Laissez un commentaire