ELECTROLYSE ET SYNTHESE DE L’EAU
Electrolyse
Expérience:
On réalise le dispositif constitué d’une cuve
électrolytique, des électrodes reliées a un circuit électrique alimenté par le
générateurs G (schéma de la figure ci-dessous). Deux tubes à essais plongent
dans la cuve, l’un a l’anode, l’autre à la cathode. Sachant que les tubes à
essais sont remplis du même liquide que celui de la cuve.
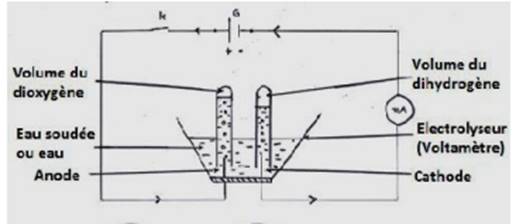
Observations:
·
Lorsque
l’interrupteur k est ouvert, on n’observe rien.
·
Lorsqu’on
ferme l’interrupteur K, on observe, le courant circule dans le circuit. On
observe:
- des dégagements gazeux au niveau des électrodes,
- Le contenu
du tube de l’anode est à un niveau plus élevé.
Interprétation:
Le passage du courant électrique a conduit a conduit à
la formation de deux gaz:
-du
dioxygène a l’anode
-du
dihydrogène a la cathode
Mise en évidence des gaz formés:
·
La flamme d’une
buchette allumée se ravive lorsqu’on la présente à l’ouverture du tube
de gauche» le gaz formé dans ce tube est le dioxygène (O2).
·
Une légère détonation
est entendue lorsqu’on présente la buchette d’allumette a l’ouverture[H1] du tube de droite. Le gaz formé est le dihydrogène
(H2)
Définition:
L’électrolyse de l’eau est la
décomposition par le courant électrique de l’eau en deux gaz: le
dioxygène(O2) et le dihydrogène(H2).
L’équation
de cette décomposition de l’eau s’écrit:
2H2O→O2
+ 2H2
Le volume du dihydrogène est le double de celui du
dioxygène lors de l’électrolyse de l’eau;
VH2=2VO2
Synthese
de l’eau
Définition:
La synthèse de l’eau est la formation de l’eau à
partir du mélange réactionnel de dihydrogène et de dioxygène.
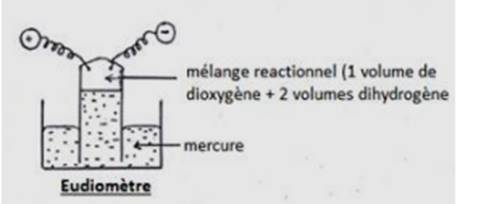
Expérience:
On retourne sur une cuve a mercure
une éprouvette contenant un mélange de dioxygène et de dihydrogène et
comportant un dispositif pouvant produire une étincelle.
Observation:
Après le passage de l’étincelle, les
gaz sont brulés et on observe:
-une diminution de pression qui se manifeste par la
montée du mercure dans l’éprouvette..
-une buée ou gouttelettes sur la paroi intérieure de
l’éprouvette.: c’est l’eau.
La combustion du dioxygène et du dihydrogène a
donc conduit à la formation de l’eau. L’équation bilan est:
2H2 + O2 → 2H2O
EXERCICES
EXERCICE I:
Lors d’une expérience sur l’électrolyse de l’eau, on a recueilli 480 cm3
de dihydrogène.
1- Sur quelle électrode a-t-on recueilli le gaz dihydrogène ?
2- Calculer le nombre de moles de dihydrogène recueilli.
3- Écrire l’équation bilan de cette réaction chimique.
4- Calculer la masse d’eau à décomposer.
On donne Vm
=24L.mol-1 ; MO = 16g.mol-1 ; MH = 1g.mol-1
EXERCICE
II:
1-Equilibrer l’équation suivante: H2O→H2+O2
2-Au cours d’une séance de travaux pratiques, on
réalise une expérience d’électrolyse de l’eau.
Le professeur fait arrêter l’expérience lorsque le
volume le plus important de gaz recueilli a l’une des électrodes atteint 20 cm3.
a-Faire le schéma annoté de l’électrolyseur.
b-Indiquer la valeur du volume de gaz recueilli à l’autre électrode.
c-Comment peut-on caractériser chacun de ces deux gaz?
EXERCICE III:
Au cours d’une électrolyse de l’eau, on a recueilli
120 ml d’un gaz à la cathode.
1-De quel gaz s’agit-il ?
2-Comment l’identifie-t-on ?
3-Calcule le volume du gaz recueilli à l’autre
électrode.
EXERCICE IV:
Amadou utilise 80cm3 de dihydrogène et
35cm3 du dioxygène pour réaliser la synthèse de l’eau.
1. Quelle est le gaz
en excès ? justifier la réponse.
2. Détermine le volume du gaz restant.
3. Ecrit l’équation-bilan de la réaction.
Avez-vous un exercice à proposer au Forum?Cliquez-ici
Merci de votre visite
Laissez un
commentaire