STRUCTURE DE
QUELQUES COMPOSES IONIQUES
Introduction
Les corps purs à l’état solide peuvent avoir;:
-une structure atomique;: un solide atomique est un assemblage
d’atomes.
-une structure moléculaire;: un solide moléculaire est un assemblage
de molécules.
-une structure ionique;: les particules constituant le cristal sont
des ions positifs et des ions négatifs.
STRUCTURE DU CHLORURE
DE SODIUM
Le chlorure de sodium est un cristal constitué d'ions sodium
et d'ions chlorures. Ce cristal ou réseau cristallin est formé de la répétition
d'une même figure géométrique appelée maille.
La maille du chlorure de sodium est cubique à faces centrées (CFC).
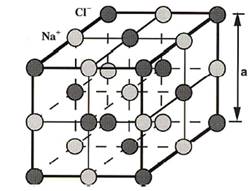
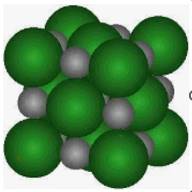
C'est un cube d'arête a=560 pm dont :
-Les sommets sont occupés par les ions Cl-
-Les centres des 6 faces sont occupés par les ions Cl-
-Les milieux des 12 arêtes sont occupées par les ions Na+
-Le centre du cube est occupé par Na+.
Dans ce
schéma, une maille est l’unité de base de la structure cristalline. C’est un
parallélépipède (souvent un cube) qui se répète régulièrement dans l’espace
pour former le cristal entier. Elle contient un certain nombre d’ions sodium
(Na⁺) et d’ions chlorure (Cl⁻) partagés avec les mailles voisines. Ici, la maille
contient en moyenne 4 ions Na⁺ et 4 ions Cl⁻, ce qui donne la formule statistique NaCl.
La maille permet donc de modéliser l’arrangement
régulier des ions dans un solide ionique. Dans le cas du chlorure de sodium (NaCl),
la maille est cubique (on parle de maille cubique à faces centrées). La
cohésion du cristal est assurée par des forces électriques entre les ions
sodium et chlorure.
FORMULES STATISTIQUES
DE QUELQUES COMPOSES
On attribue
aux solides ioniques une formule statistique, qui est une formulé de
composition dans laquelle n’apparait pas la charge de l’ion. L’ion positif
s’écrit toujours avant l’ion négatif. Ainsi la formule du chlorure de sodium
solide s’écrira NaCl,
car pour un ion sodium il y a un ion chlorure.
La formule statistique d’un solide cristallin (comme
un sel ionique) indique le rapport en nombre d’ions ou d’atomes présents dans
une maille élémentaire du cristal. Elle ne donne pas le nombre exact total
d’ions dans tout le cristal (car il en contient un très grand nombre), mais le
rapport minimal entier entre les ions ou atomes dans la maille.
Exemple;:
Ecrivons la formule statistique du sulfate
d’aluminium sachant qu’il est constitué d’ions sulfate SO2-4
et d’ions aluminium Al3+.
La formule s’écrira;: Alx(SO4)y
Il faut déterminer x et y. la neutralité électrique
impose que 3x=2y. on prend les plus petites valeurs de x et y satisfaisant
cette relation, soit;: x=2 et y=3
d’où la formule
cherchée;: Al2(SO4)3
EXERCICES
EXERCICE I:
1.Le cristal de
chlorure de sodium possède une structure cubique à faces centrées.
Chaque maille
élémentaire contient :
- des ions Na⁺ aux centres des arêtes et au centre de
la maille,
- des ions Cl⁻ aux sommets et aux centres des faces.
a) Combien y
a-t-il d’ions Na⁺ par maille ?
b) Combien y
a-t-il d’ions Cl⁻ par maille ?
c) Quelle est
la formule statistique du cristal ?
2.On considère
la maille cubique du cristal de NaCl.
Les masses
molaires sont : Na = 23 g/mol, Cl = 35,5 g/mol.
La constante
d’Avogadro est NA = 6,02 × 10²³ mol⁻¹.
a) Quelle est
la masse d’un ion Na⁺ et d’un ion Cl⁻ ?
b) En déduire
la masse d’une maille.
3.La maille
cubique de NaCl
a une arête de a = 564 pm (1 pm = 10⁻¹² m).
Utiliser la
masse d’une maille pour calculer la masse volumique du cristal.
EXERCICE II : Oxyde de magnésium (MgO)
Le
cristal est formé de Mg²⁺ et O²⁻.
a) Combien
faut-il d’ions Mg²⁺ pour équilibrer un ion O²⁻ ?
b) Quelle est
la formule statistique du cristal ?
EXERCICE III : Fluorure de calcium (CaF₂)
Le
cristal est constitué de Ca²⁺ et F⁻.
a) Quel est le
rapport ionique nécessaire pour que le cristal soit électriquement neutre
?
b) En déduire
la formule statistique.
Avez-vous un exercice à proposer au Forum?Cliquez-ici
CORRIGES Merci de votre visite
Laissez un
commentaire