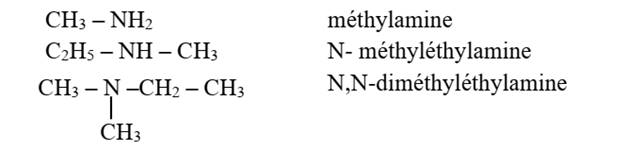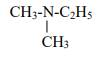LES AMINES
DEFINITION
ET NOMENCLATURE
. Une amine résulte du remplacement d’un ou plusieurs atomes
d’hydrogène dans la molécule d’ammoniac (NH3) par un ou plusieurs
groupements alkyles ou aryles.
Ainsi, les amines saturées ont pour formule brute générale CnH2n+3
N.
Les trois classes d’amine
Il existe trois classes d’amines selon que l’atome d’azote porte un, deux ou trois groupes akyles ou aryles. Elles sont appelées respectivement amines primaires, amines secondaires et amines tertiaires de formules générales.
Les radicaux R1, R2, R3 peuvent être
identiques ou différents: ce sont les amines aliphatiques. Si le radical
est groupe aryle, l’amine est dite aromatique.
Nomenclature des amines
Première méthode :
- Les amines sont nommées en remplaçant le « e » final de l’alcane dont elles
proviennent par « amine »
avec indice de position du groupe NH2.
- L’atome de carbone lié à l’atome d’azote porte le numéro 1.
- Si l’amine est secondaire ou tertiaire, on énonce les autres groupes devant,
précédés de la lettre N ou des
lettres N, N.
Exemple:
Deuxième méthode
- Les amines primaires sont nommées en alkylamines où le groupe alkyle est la
partie liée au
groupe NH2.
- |
Si l’amine est secondaire ou tertiaire, on énonce les autres groupes devant, précédés de la lettre N ou N, N |
Exemple:
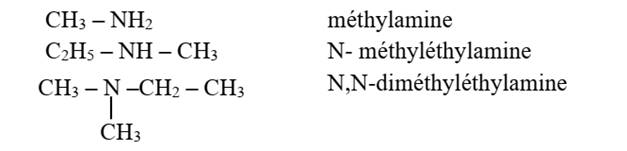
PROPRIETES
CHIMIQUES DES AMINES
Caractère basique des amines
Les amines sont des bases faibles du fait du doublet non liant sur l’atome
d’azote.
R-NH2 + H2O ⇌R-𝑁+H3
+ HO-
Caractère nucléophile des amines
Le doublet non liant de l’azote confère aux amines un caractère nucléophile.
*Réaction d’Hofmann (alkylation des amines).
L’azote (centre nucléophile) attaque le carbone (centre électrophile) dans la
molécule halogénée R-X
(X=I, Br, Cl…).
· Cas d’une amine tertiaire
Une amine tertiaire réagit avec un dérivé halogéné pour donner un ion ammonium quaternaire stable appelé ion alkylammonium.
Exemple : L’alkylation de la N, N-diéthyléthylamine.
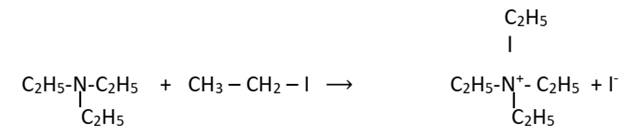
· Cas des amines primaires et secondaires
L’action d’une amine primaire sur un dérivé halogéné conduit à la formation successive des amines secondaires et tertiaires, et finalement, à celle d’un ion ammonium quaternaire.
EXERCICES
EXERCICE I:
A- Nomme les amines suivantes :
a)
b) CH3-NH-CH2-C2H5
B-Écris la formule semi-développée des amines suivantes :
a) N-éthyl-N-méthylpropanamine
b) N-méthyléthanamine
EXERCICE II.
Une amine de formule brute C4H11N :
1. Écris les formules semi-développées possibles ;
2. Nomme-les, puis précise leur classe.
EXERCICE III:
Des amines primaires saturées et non cycliques contiennent n atomes de carbone.
1. Donner leur formule brute en fonction de n.
2. Une masse de 15 g de l’une de ces amines contient 2,9g d’azote. Déterminer sa formule brute, ainsi que les formules semi-développées de tous ses isomères possibles.
EXERCICE IV:
Une amine tertiaire contient une masse de 66% de carbone, 15% d’hydrogène et 19% d’azote.
1. Déterminer sa masse molaire.
2. Donner sa formule brute, sa formule semi-développée ainsi que son nom.
3. Quelle est la masse du produit obtenu lorsqu’on fait réagir 0,73 g de l’amine sur 1,56 g d’iodoéthane, en supposant la réaction totale.
EXERCICE V:
Une amine a pour formule brute; C8H11N.
1. Donner les formules semi-développées et les noms de tous ses isomères amines.
2. Identifier les formules des isomères aromatiques.
3. L’amine précédente réagit sur l’iodoéthane pour donner un seul produit. Donner la formule et le nom de cet amine et du produit formé.
EXERCICE VI:
Une amine tertiaire A réagi sur l’iodo-1-butane en solution dans l’éther, pour donner un précipité blanc qui est un solide ionique.
1. Ecrire l’équation bilan de la réaction.
2. Quelle est la propriété des amines que cette réaction met en évidence?
3. Une solution de l’amine A, de concentration C=0,2 mol.l-1, est obtenue par dissolution de 20,2 g d’amine pour 1l de solution. En déduire sa masse molaire, sa formule brute, sa formule semi-développée et son nom.
EXERCICE VII:
La masse molaire d’une amine saturée non cyclique est de 59 g/mol.
1. Déterminer la formule brute de cette amine.
2. Donner les formules développées possibles, les noms et les classes des amines correspondantes.
3. Ecrire l’équation de la réaction de l’une des amines avec l’eau. Quels caractères des amines cette réaction met – elle en jeu
4. Une de ces amines réagit avec l’iodure d’éthane en donnant un seul produit. Ecrire l’équation bilan de cette réaction et nommer le produit obtenu. Quel caractère des amines cette réaction met-elle en jeu? Le définir.
Données; O: 16; N: 14; H:1
Avez-vous un exercice à proposer au Forum?Cliquez-ici
Merci de votre visite
Laissez un commentaire