MOLECULES ET NOTION DE VOLUME MOLAIRE
Définitions
· Une liaison covalente entre deux atomes est la mise en commun d’un doublet d’électron.
Exemple:
L’atome d’hydrogène, dont la couche externe n’est pas saturée ne peut pas exister seul’ il s’associe a un autre atome d’hydrogène: ces deux atomes mettent en commun leurs électrons.
La représentation de Lewis de la molécule de dihydrogène est la suivante
H-H
Une molécule est un assemblage, électriquement neutre, formé des atomes liés entre eux par des liaisons covalentes.
Exemple
La molécule d’eau : H2O
· L’atomicité d’une molécule est le nombre d’atome qu’elle renferme.
Exemple :
L’atomicité de la molécule d’eau est 2’
Remarques :
-Les électrons qui peuvent être mis en commun sont des électrons célibataires. Le doublet d’électron qu’ils forment est un doublet liant, par opposition au doublet non liant pouvant exister sur la couche externe d’un atome.
-Un atome peut former autant de liaisons covalentes qu’ils possèdent des électrons célibataires sur sa couche externe.
-Le nombre de liaisons covalentes que peut former un atome est la valence de cet atome.
Représentations d’une molécule
Formule brute, représentation de Lewis, formule développée
La formule brute d’une molécule est obtenue par juxtaposition des symboles des éléments constituant la molécule. Chaque symbole porte en indice, en bas et à droite, le nombre d’atomes de cet élément dans la molécule. Le nombre 1 n’est pas porté.
Exemples : H2O; HCl
La représentation de Lewis met en évidence les doublets liants et non-liants.
Formule développée (ou représentation de Lewis simplifiée) ne met en évidence que les doublets de liaison.
Exemples : H-Cl pour HCl; Cl-Cl pour Cl2
Structure géométrique d’une molécule
La stéréochimie est la partie de la chimie qui traite de la structure géométrique des molécules. Pour représenter la structure géométrique des molécules, les chimistes utilisent des modèles moléculaires. Il en existe deux types :
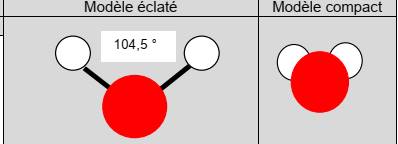
-modèles éclatés : des petites boules représentent les centres des atomes. Les tiges reliant les boules symbolisent les liaisons.
-modèles compacts : les boules, plus grosses représentent les centres des atomes. Leurs rayons sont proportionnels a ceux des atomes
Exemple: pour la molécule H2O
2.Autre type de liaison chimique : liaison ionique
Elle se forme par transfert d’électrons d’un atome vers un autre.
· Un atome perd un ou plusieurs électrons → ion positif (cation)
· Un autre atome gagne ces électrons : ion négatif (anion)
· L’attraction électrostatique entre les ions forme la liaison
Exemple : NaCl (chlorure de sodium)
4.Le volume molaire : loi d’Avogadro-Ampère
Loi d’Avogadro-Ampère
Dans les mêmes conditions de température et de pression, le volume occupé par une mole de gaz est indépendant de la nature de ce gaz. On l’appelle volume molaire, noté Vm.
Dans les conditions normales de température et de pression (0°C 1,013Pa), le volume molaire vaut 22,4 l.mol-1
Détermination d’une quantité de matière pour les gaz :
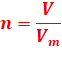
Vm: Volume molaire (l.mol-1)
V: Volume de l’échantillon(l)
n: quantité de matière (n)
Loi des gaz parfaits
Ø Loi de Boyle-Mariote: A température constante, pour une masse donnée de gaz, le produit de la pression du gaz par son volume est constant:
TV=K, K étant une constante
Ø Loi de Gay-Lussac : A pression constante, le volume d’une masse donnée de gaz est proportionnel à la température absolue:
V/T =constante, a pression constante
Avec T(K)= t(![]() C)+273
C)+273
ØLoi de Charles : A volume constant, la pression d’une masse de gaz donne est proportionnelle a la température absolue
P/T=constante, a volume constant.
Définition :
Un gaz parfait est un gaz qui suit à toute température et sous toute pression les lois de Boyle-Mariote, Gay-Lussac et Charles.
On a :
PV=nRT
n : nombre de moles (mol);
V : volume(m3)
P: pression (Pa)
T : température(K)
R est la constante des gaz parfaits
R=8,31 unités S.I
Relation entre la masse molaire et la densité d’un gaz
Dans les CNTP, une mole une mole occupe 22,4l. la masse d’air qui occupe le même volume est 1,293x22,4=29 g puisque la masse volumique de l’air vaut 1,293g/l. Pour les gaz,
![]()
d: densité
M: masse molaire(g/mol)
EXERCICES
EXERCICE I:
1.
Donner la définition d’une molécule
2. Comment se forme une liaison covalente ?
3. L’atome de carbone C peut former 4 liaisons covalentes.
3.1 A quelle règle obéit-il ?
3.2 Donner les différentes possibilités d’obtenir 4 liaisons covalentes avec
l’atome de carbone.
4. Donner la structure géométrique de HCl en modèle éclaté et compact.
5. Donner les représentations de Lewis de: Cl2H2O et NH3
EXERCICE
II:
1) Déterminer la quantité de matière n d'un échantillon contenant : 4,86x1021
atomes de carbone et 8,35x1024 molécules d'eau
2)
Déterminer le nombre N d'entités contenues dans les échantillons suivants
. a) 5,00x10-3 moles de cuivre
. b) 12 moles
de dioxyde de carbone
NA=6,023.1023 est le nombre d’Avogadro
EXERCICE III:
On considère un échantillon de 1,6g de soufre.
1. Quelle quantité de matière renferme cet échantillon ?
2. Quel nombre d’atomes contient-il ?
3.Au cours de la combustion d’un morceau de soufre, on a recueilli 100 cm3 de dioxyde de soufre (SO3), volume mesuré dans les conditions pour lesquelles le volume molaire vaut 25l.
3.1 Quelle quantité de matière renferme ce volume gazeux ?
3.2 Quelle est la masse du gaz ?
On donne H: 1 N: 14 O: 16
EXERCICE IV:
L’ammoniac est un gaz de formule chimique NH3
1. Quelle quantité de matière renferme 3,4 g d’ammoniac?
2. Quel est le volume occupé dans les conditions normales par 3,4 g d’ammoniac ?
3. Quel sera son volume en litre s’il contient0.5 moles de quantité de matière ?
Volume mesuré dans les conditions où le volume molaire vaut 25 l.
EXERCICE V:
L’Aspirine ou acide acétylsalicylique à pour formule brute: C9H8O4.
1- Déterminer sa masse molaire.
2- Calculer la quantité de matière contenue dans un comprimé d’Aspirine 500 (un comprimé à une masse de 500 mg).
EXERCICEVI:
La formule d’un composé peut s’écrire: CxHyO
L’analyse montre que ce corps contient en masse, 62,1% de carbone et 10,3% d’hydrogène.
1. Déterminer le pourcentage en masse de l’oxygène.
2. En déduire la masse molaire du composé
3. Trouver la formule du composé.
EXERCICEVII:
1.Un gaz parfait occupe un volume de 4,0 L sous une pression de 1,0 × 10⁵ Pa à la température de 27 °C..Calculer la quantité de matière du gaz.
2.On enferme 2,8 g d’azote (N₂) dans un récipient de volume 2,0 L à la température de 27 °C.
2.1. Calculer la quantité de matière du gaz.
2.2. Déterminer la pression du gaz.
(Donnée : masse molaire de N₂ = 28 g·mol⁻¹)
3.Un gaz parfait occupe un volume de 3,0 L à la température de 27 °C sous une pression de 1,5 × 10⁵ Pa.
3.1. Calculer la quantité de matière du gaz.
3.2.
On porte la température à 127 °C, le volume restant constant.
Calculer la nouvelle pression.
Avez-vous un exercice à proposer
?Cliquez-ici
Merci de votre visite
Laissez un commentaire