ALDÉHYDES ET CÉTONES
DÉFINITIONS
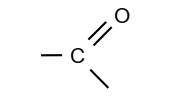
✓ Un composé
carbonylé est un composé organique oxygéné comportant le groupe carbonyle :
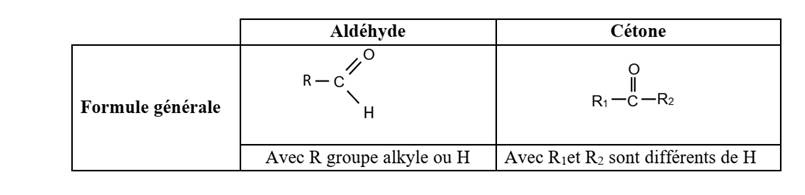
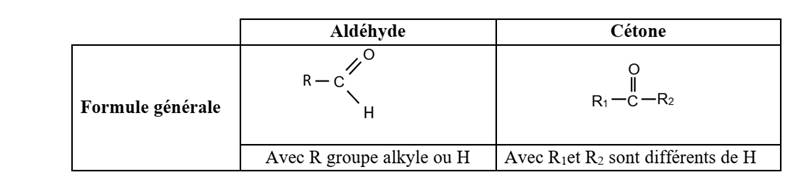
Un aldéhyde est un composé carbonylé dont l’atome de carbone du groupe
carbonyle est lié à un atome d’hydrogène.
Une cétone est un composé carbonylé dont l’atome de carbone du groupe carbonyle est lié à deux atomes de carbone tétragonaux.
Formule
brute générale: CnH2nO, où n est
le nombre d’atomes de carbone.
NOMENCLATURE
Nomenclature des aldéhydes
Le nom d’un aldéhyde s’obtient en remplaçant le «e» final du nom de l’alcane dont il dérive par le suffixe «al». Dans les aldéhydes, le groupe carbonyle est toujours situe en bout de chaine; il est inutile de préciser la position du carbone fonctionnelle revanche, la position des éventuels substituants est aussi précisée en numérotant la chaine carbonée (la plus longue) à partir du carbone fonctionnel du groupe aldéhyde.
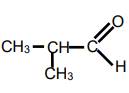
Exemple:
2-methylpropanal
Nomenclature des cétones
Le nom d’une cétone s’obtient en remplaçant le «e» final du nom de l’alcane dont il dérive par le suffixe «one», précédé d’un indice précisant la position du carbone fonctionnel dans la chaine carbone principale (la plus longue), est numérotée de façon à attribuer au carbone fonctionnel le plus petit indice possible.
Exemple:
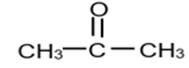
Propan-2-one ou Propanone
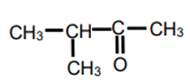
3-méthylbutan-2-one
PROPRIÉTÉS
CHIMIQUES
Les aldéhydes et les cétones possèdent une propriété commune: l’action sur la 2,4-dinitrophenylhydrazine(2,4-D.N.P.H). Contrairement aux cétones, les aldéhydes peuvent subir l’oxydation ménagée, ce qui leur confère un caractère réducteur.
Propriété
commune (Test commun) : test à la Dinitrophénylhdrazine
En présence d’un composé carbonylé (aldéhyde et cétone), la 2,4-dinitrophénylhydrazine (2,4-DNPH)
donne un précipité jaune-orangé.

Propriétés
spécifiques aux aldéhydes
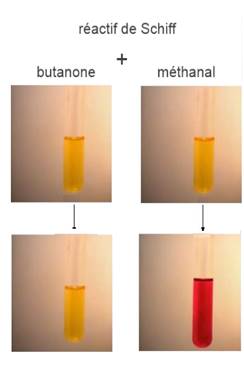
Test au réactif de Schiff
En présence d’un aldéhyde, le
réactif de Schiff (incolore) vire
au rose.
Propriétés
réductrices des aldéhydes
Test au nitrate d’argent ammoniacal (ou réactif de Tollens)
Les aldéhydes réduisent le réactif de Tollens.
Au cours cette réaction, en milieu basique, l’aldéhyde est oxydé
en ion carboxylate et l’ion diamine argent I (présent dans le
réactif de Tollens) est réduit en argent métallique.

L’équation-bilan de cette oxydo-réduction s’écrit :
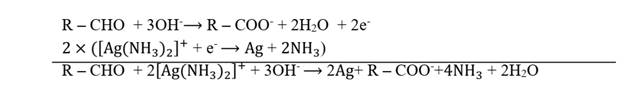
Réduction
de la liqueur de Fehling
Les aldéhydes réduisent la liqueur de
Fehling.
Au cours de cette réaction, les ions
cuivre II (présent dans la liqueur de
Fehling) sont réduits en oxyde de
cuivre I et l’aldéhyde est oxydé en ion
carboxylate.
L’équation-bilan de cette oxydo-réduction s’écrit :
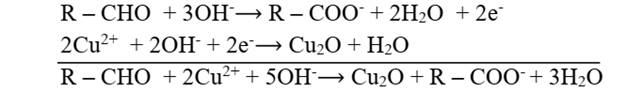
Conclusion
· Le dépôt d’argent avec le réactif de Tollens et la formation du précipité rouge brique avec la liqueur de Fehling met en évidence la présence du groupe aldéhyde.
· Les aldéhydes sont des réducteurs, ce qui n’est pas le cas des cétones.
|
|
2,4-DNPH |
Réactif de Schift |
Réactif de Tollens |
Liqueur de Fehling |
Aldéhyde |
Précipité jaune |
Coloration rose |
Formation du miroir d’argent |
Précipité rouge brique de Cu2O |
cétone |
Précipité jaune |
rien |
Rien |
rien |
EXERCICES
EXERCICE I:
1. Une solution contient du propanal et de la propanone. Comment pourrait-on mettre en évidence chacun des deux composés?
2. Un composé de formule C3H6O donne un précipité jaune avec la 2,4-D.N.P.H, mais ne réagit pas avec le réactif de Tollens. En déduire la formule semi-développée et le nom de ce composé.
3. Un composé A présente les propriétés suivantes: A rosit le réactif de Schiff et donne un précipité jaune avec la 2,4-D.N.P.H. D’autre part, 1 g de A traité avec un excès de l’ion complexe Ag (NH3)2+ donne un dépôt de 3,72 g d’argent. En déduire la formule de A.
EXERCICE II:
Tu disposes d’un composé carbonylé A de formule brute C2H4O.
1. Donne :
1.1. La fonction chimique et le groupe fonctionnel de A ; 1.2. La formule semi-développée et le nom de A ; 2. Précise ce qu’on observe quand on fait réagir A avec : 2.1. Une solution de 2,4-DNPH ; 2.2. Le réactif de Tollens. 3. Écris l’équation-bilan de la réaction du composé A avec la liqueur de Fehling (Cu2O/Cu2+)
EXERCICE III:
Au laboratoire de Physique-Chimie de ton établissement scolaire, se trouve une bouteille d’alcool saturé A qui porte la mention unique suivante : densité de vapeur par rapport à l’air d = 2,07. Le professeur te demande de définir cet alcool et le produit B de son oxydation ménagée en milieu acide par les ions dichromates Cr2O7 2− , sachant que B réagit avec la 2,4-D.N.P.H et possède des propriétés réductrices.
1. Donne la formule générale d’un alcool saturé dont la formule renferme n atomes de carbone.
2. Montre que la formule brute de l’alcool A est C3H8O. 3. Détermine la fonction chimique de B.4. Déduis-en les formules semi-développées et les noms de A et B.
Données : C : 12 gmol−1 ; O : 16 gmol−1 ; H : 1 gmol−1EXERCICE IV:
La combustion complète de 0,770 g d’une substance organique formé du carbone, d’hydrogène et d’oxygène donne 0,630g d’eau et 1,54g de dioxyde de carbone.
1. Quelle est la composition centésimale de cette substance?
2. Quelle est sa formule brute, sachant que sa densité de vapeur par rapport à l’air est voisine de 1,5?
3. Déterminer la formule développée de cette substance sachant qu’elle donne un précipité jaune avec la 2,4-D.N.P.H. et qu’elle réduit la liqueur de Fehling.
EXERCICE V:
69 g d’éthanol est traité de façon à obtenir de l’éthanal. 1. Quelle masse maximale peut-on espérer obtenir? 2. On prélève 1/100 du liquide obtenu et on traite par la liqueur de Fehling. Le précipité rouge obtenu, lavé et séché, pèse 1,27g. Quel a été le rendement de la transformation de l’éthanol en éthanal
Avez-vous un exercice à proposer au Forum?Cliquez-ici
Merci de votre visite
Laissez un commentaire