CORRIGES :
EXERCICE I:
1. Mise en évidence de chacun des deux composés
Utiliser
-soit le Réactif de Schiff qui donne une coloration rose avec le propanal et rien avec la propanone.
-soit le Réactif de Tollens qui donne la formation d’un miroir d’argent avec le propanal et rien avec la propanone.
-soit la Liqueur de Fehling qui donne un Précipité rouge brique de Cu2O avec le propanal et rien avec la propanone.
2. Il s’agit de la formule propanone.
Formule semi-développée:
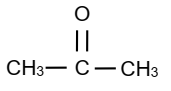
3. Le composé Aest un aldéhyde de formule générale: CnH2nO.
Sa masse molaire est M=12n+2n+16=14n+16
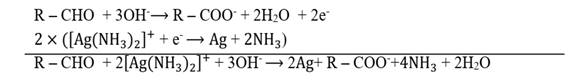
Soient nA, nombre de moles de A et nAg, nombre de moles de Ag.
![]() <=>
<=>![]() =>n=3 =>C3H6O
=>n=3 =>C3H6O
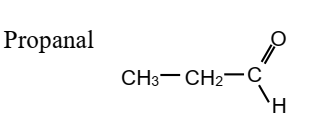
EXERCICE II:
1. Donnons :
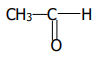
1.1. Fonction chimique : Aldéhyde ; groupe fonctionnel : -CHO ou
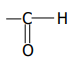
1.2. Formule semi-développée :
2. 2.1. Précipité jaune
2.2. Miroir d’argent ou dépôt d’argent
3. Équation-bilan avec la liqueur de Fehling
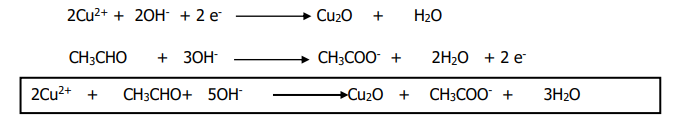
EXERCICE III:
Formule générale d’un alcool saturé CnH2n+1OH ou CnH2(n+1)O
2. Formule brute de l’alcool
La masse molaire de A est MA = 29d = 60 gmol−1
MA = (12n + 2n + 2 + 16 )/60 = 14 n + 18 n = 3 D’où la formule brute C3H8O .
3. La fonction chimique de B. B réagit avec la 2,4-D.N.P.H et possède des propriétés réductrices ; B est un aldéhyde.
4. Les formules semi-développées et les noms de A et B.

Puisque B est un aldéhyde, alors A est l’alcool primaire de formule CH3 − CH2 − CH2 − OH nommé propan-1-ol.
B est le Propanal E
EXERCICE IV:
2.1. Composition centésimale de cette substance
%C=(mc/m) x100 or mC =(12x1,54) /44=0,42 => %C= (0,42/0.770) x100=54,54% // tout le carbone de la substance est contenu dans le CO2.
%H=(mH/18) x100 or mH =(2x0,630) /18=0,07 => %H= (0,07/0.770) = x100=9,09% // tout l’hydrogène de la substance est contenu dans le H2O.
%O=100-(54,54+9,09) = 36,36%
2.2. Formule brute,
M=29d=29x1,5=43,5g mol-1
14n+16=43,5 => n![]() 2 =>C2H4O
2 =>C2H4O
2.3. Formule développée:
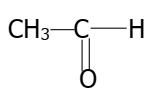
.
EXERCICE V:
1. l’oxydation de l’éthanol au contact du cuivre chaud donne de l’éthanal selon l’équation:
CH3-CH2-OH +1/2O2→CH3-CHO +H2O
La réaction se fait mole a mole en présence du CuCH3-CHO
![]() =
=![]()
![]()
2. L’équation bilan avec la liqueur de Fehling est:
CH3-CH2-OH +2Cu2+ +5HO- →Cu2O + CH3-COO- +3H2O
![]() =
=![]()
![]() =
=![]()
![]()
![]()