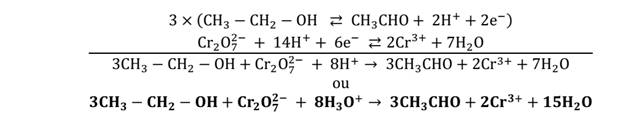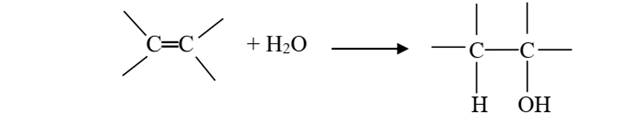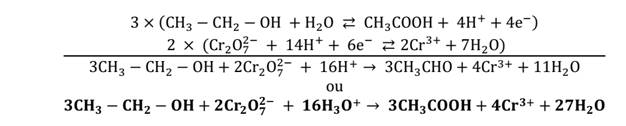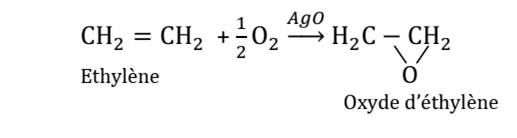LES ALCOOLS
DEFINITION ET
NOMENCLATURE
Définition
On appelle alcool un composé organique possédant un groupe hydroxyle (–OH) lié
à un atome de carbone tétragonal. Tous les alcools possèdent un groupe d’atome
appelé groupe fonctionnel de formule C–OH. Le carbone qui porte le groupe
hydroxyle est appelé carbone fonctionnel. Il est tétragonal car il est lié
quatre atomes voisins par des liaisons covalentes simples.
Formule
générale des alcools : R–OH avec R groupement alkyle de formule CnH2n+1.
Formule
brute
: CnH2n+2 O avec (n≥ 1).
Nomenclature
Le nom d’un alcool dérive du nom de
l’hydrocarbure qui lui a donné naissance : il est obtenu en remplaçant le « e »
final par le suffixe « ol ».
-La chaine
carbonée la plus longue (chaine principale) est celle qui passe par le carbone
fonctionnel.
-le sens de numérotation des atomes de carbone de la chaine est celui
qui permet d’affecter le numéro le plus bas possible au carbone fonctionnel.
-La position
du groupe -OH est indiquée par un tiret, suivi du numéro du carbone
fonctionnel.
-Les substituants sont cités dans l’ordre alphabétique, les préfixes
multiplicatifs di, tri…ne sont pas pris en compte.
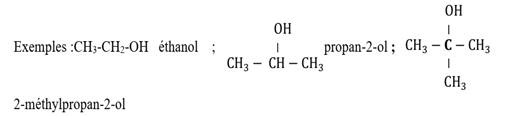
Exemple:
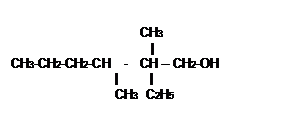 2-ethyl,2-3dimethylhexan-1-ol
2-ethyl,2-3dimethylhexan-1-ol
LES 3 CLASSES
D’ALCOOL
.
Les alcools, regroupés en trois classes, se distinguent par le nombre d’atomes
de auxquels ils sont directement liés. Ainsi, lorsque le carbone fonctionnel
est liéà:
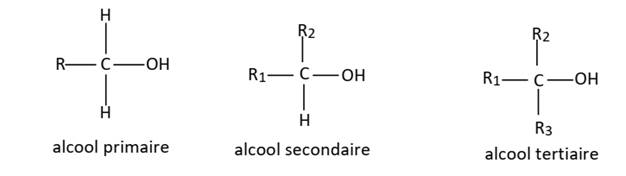
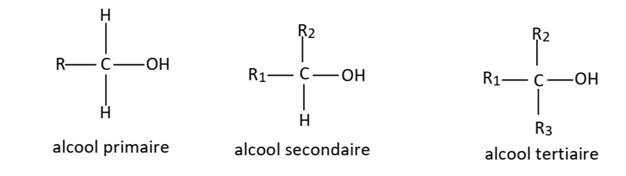
-0 ou1atome de carbone, l’alcool est primaire.
-2 atomes de carbone, l’alcool est secondaire. -3
atomes de carbone, l’alcool est tertiaire.
PROPRIETES
CHIMIQUES DES ALCOOLS
Réaction
avec le sodium
. L’alcool réagit avec le sodium pour donner un
alcoolate de sodium.

Déshydratation
d’un alcool
- La déshydratation intramoléculaire conduit à un alcène. Elle se fait en
milieu acide (sulfurique).
Al2O3 : alumine
- La déshydratation intermoléculaire conduit à un étheroxyde
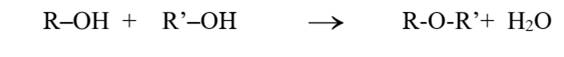
Combustion
des alcools
-Elle produit du dioxyde de carbone et de l’eau. Elle
s’accompagne d’une destruction de la chaine carbonée.
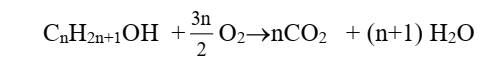
Oxydation
ménagée des alcools
L’oxydation ménagée s’effectue
sans destruction de la chaîne carbonée.
Cas des
alcools primaires
. Un alcool
primaire s’oxyde pour donner un aldéhyde si l’oxydant est en défaut ou un acide
carboxylique si l’oxydant est en excès. 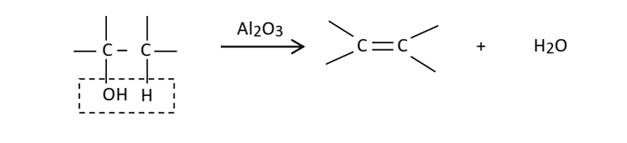
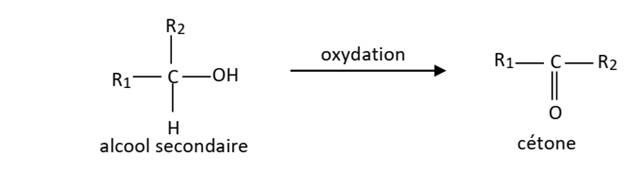
Cas des
alcools secondaires
Ils sont oxydables en cétone.
Cas des
alcools tertiaires
Les alcools tertiaires ne sont pas oxydables.
Oxydation
en solution aqueuse
Avec un
alcool primaire
L’oxydation de l’éthanol en milieu acide par le dichromate de potassium donne
l’éthanal. C’est une réaction d’oxydoréduction en milieu acide.
Equation bilan de la réaction est :
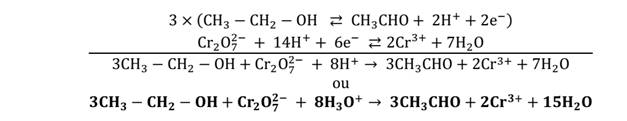
Réaction de l’oxydation de l’éthanol par une solution de dichromate
de potassium en excès. On obtient un acide carboxylique.
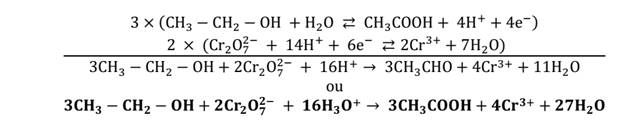
Avec un
alcool secondaire
La réaction de l’oxydation de l’éthanol par une solution de
dichromate
de potassium en excès donne une cétone.
L’oxydation du propan-2-ol en milieu acide donne la propanone. 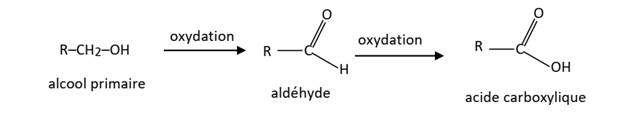
-L’oxydation ménagée
d’un alcool tertiaire est impossible.
Estérification
L’estérification est l’action d’un acide carboxylique sur un alcool.
Elle conduit à la formation d’un ester et de l’eau, suivant
l’équation-bilan:
 L’expérience
montre que cette réaction est lente et athermique. Elle est limitée par la
réaction inverse appelée hydrolyse de l’ester qui se produit dans les mêmes
conditions. On aboutit à un équilibre chimique qui se traduit par une double
flèche. Le mélange réactionnel contient alors les quatre composes: acide,
alcool, ester et eau, dans des proportions bien définies, variables avec la
classe d’alcool. Par
élévation de température ou l’utilisation d’un catalyseur (exemple:H2SO4),
on peut rendre l’estérification plus rapide, sans modifier l’équilibre
chimique.
L’expérience
montre que cette réaction est lente et athermique. Elle est limitée par la
réaction inverse appelée hydrolyse de l’ester qui se produit dans les mêmes
conditions. On aboutit à un équilibre chimique qui se traduit par une double
flèche. Le mélange réactionnel contient alors les quatre composes: acide,
alcool, ester et eau, dans des proportions bien définies, variables avec la
classe d’alcool. Par
élévation de température ou l’utilisation d’un catalyseur (exemple:H2SO4),
on peut rendre l’estérification plus rapide, sans modifier l’équilibre
chimique.
Saponification
Réaction de
saponification
La réaction des esters sur les bases fortes telle que la soude ou la
potasse conduit à un carboxylate de sodium ou de potassium suivant la réaction
d’équation bilan générale: 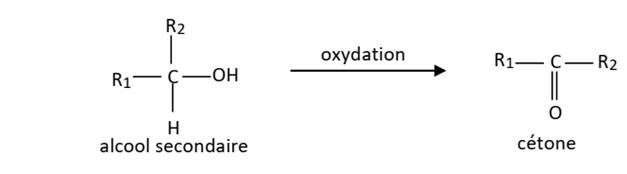
Corps gras
Les corps gras sont des triesters provenant de la réaction d’un acide
gras (acide carboxylique) avec le glycérol. On les appelle aussi des
triglycérides (formes par une réaction d’estérification). Les
triglycérides sont des triesters, molécules possédant 3 fonctions ester
(formule ci-dessous). Ils sont présents dans tous les corps gras (huile,
graisses animales ou végétales). 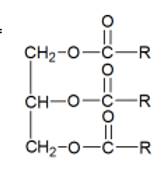
Saponification
des triglycérides par la soude L’équation-bilan de saponification des
triglycérides par la soude s’écrit donc:
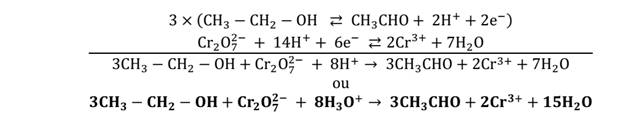
METHODE DE
PREPARATION DES ALCOOLS
Par fermentation
des jus sucrés
. La fermentation du
glucose (C6H12O6) en présence d’enzymes donne
l’éthanol.
C6H12O6⟶ C2H5OH
+ CO2
Un sucre fermentescible est un sucre qui peut fermenter sous l'action des
levures, et donc de produire de l’alcool.
Exemple : Le glucose, le saccharose et le fructose sont des sucres
fermentescibles.
Un sucre non fermentescible est un sucre non susceptible de fermenter sous
l’action des levures.
Exemples : le lactose dans le lait, l’amidon, le sorbitol…
Par hydratation des alcènes
L’hydratation d’un
alcène conduit à un alcool. 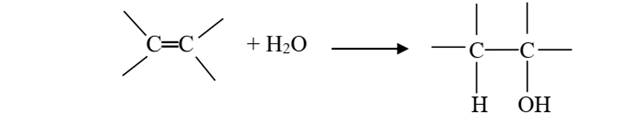
L’hydrogène se fixe sur le carbone le plus hydrogéné. C’est la règle de
Markovnikov.
LES
POLYOLS
Définition
Les polyols (ou polyalcools)
sont des alcools présentant plusieurs groupes d’hydroxyles dans leurs
structures.
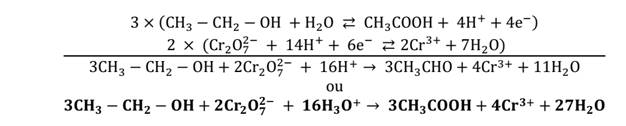
Nomenclature
On utilise les terminaison diol, triol,…
Glycol ou ethane-1,2-diol Glycérol ou
propane-1,2,3-triol Synthèse:
Le glycol se prépare en deux étapes :
- 1ère étape : oxydation de l’éthylène par le dioxygène de l’air. On obtient
l’oxyde d’éthylène. 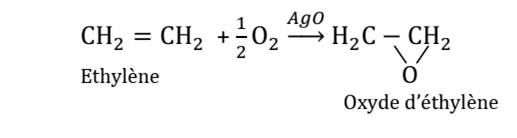
- 2ème étape : hydratation de l’oxyde d’éthylène pour obtenir le glycol.

Utilisationdes polyols :
-fabrication des mousses
-additifs alimentaires
EXERCICES
EXERCICE I :
On
effectue l’oxydation de deux alcools isomères de formule brute: C3H8O.
1. Donner le nom, la formule semi-développée et la classe de chacun des
deux isomères.
2. Donner la nature, le nom et la formule semi-développée des produits
chimiques formés lors de l’oxydation ménagée de ces deux alcools.
EXERCICE II
: Un composé A de masse molaire M =88g.mol-1 a la
composition en masse suivante: 68,20% de carbone ,13,65% d’hydrogène et
18,15% d’oxygène.
1. En déduire la formule brute. 2. Le composé A est un
alcool primaire comportant un carbone trisubstitué.
Quelle est la formule semi-développée de cet alcool ainsi que son
nom?
EXERCICE III
: On réalise la combustion complète de 6 g d’un alcool à
identifier. On obtient 7,2 g d’eau et 13,2g d’un gaz absorbable par la potasse.
1. Déterminer la composition massique de cet alcool. 2.
En déduire la masse molaire. 3. Quelle est sa formule brute?
4.
Sachant qu’il est obtenu majoritairement par hydratation de l’alcène
correspondant, identifier l’alcool étudié.
EXERCICE IV :
Le
fonctionnement de l’alcootest est basé sur le changement de couleur observe
lors de l’oxydation de l’éthanol en acide éthanoïque par le dichromate de
potassium en milieu acide. 1-Quels sont les deux couples redox mis
en jeu? 2-En déduire l’équation-bilan de la réaction intervenant
dans l’alcootest.
3-Sur un individu en état d’ivresse, on fait un prélèvement de 10 ml de
son sang auquel on aoute, en milieu acide, une solution de dichromate de
potassium en excès, de 20 cm3 contenant 14,7 g de dichromate de
potassium par litre. Apres un temps suffisamment long, on dose la solution
obtenue et on trouve que la concentration molaire du dichromate de potassium
est de 0,024 mol.l-1. Calculer la concentration en
grammes par litre de l’éthanol présent dans le sang de l’individu au moment du
prélèvement.
EXERCICE
V:
A. L’huile d’olive contient principalement de l’oléine, qui est le
triester du glycérol et de l’acide oléique. 1-Ecrire la formule
semi-développée du glycérol (propene-1,2,3-triol).
2-Determiner les formules brute et semi-développée de l’oléine. B.
On fait réagir une tonne d’oléine avec la soude en excès’ 1-Comment
appelle-t-on la réaction entre un triester et la soude? Ecrire son
équation bilan et nommer les produits de cette réaction.
2-Determiner la masse de savon obtenue sachant que la réaction est
totale. Données: Masses molaires: de
l’oléine:884g/mol ; de l’oléate de sodium:304 g/mol; de la
soude:40 g/mol.
Avez-vous
un exercice à
proposer au Forum
? Cliquez-ici
Suivez-nous sur notre page Facebook
Merci
de votre visite
Laissez un commentaire


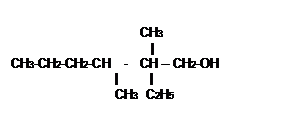 2-ethyl,2-3dimethylhexan-1-ol
2-ethyl,2-3dimethylhexan-1-ol


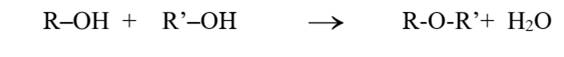
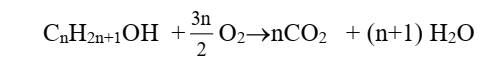


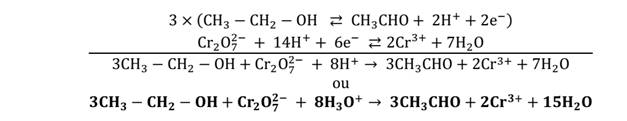
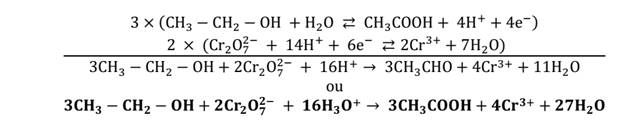

 L’expérience
montre que cette réaction est lente et athermique. Elle est limitée par la
réaction inverse appelée hydrolyse de l’ester qui se produit dans les mêmes
conditions. On aboutit à un équilibre chimique qui se traduit par une double
flèche. Le mélange réactionnel contient alors les quatre composes: acide,
alcool, ester et eau, dans des proportions bien définies, variables avec la
classe d’alcool. Par
élévation de température ou l’utilisation d’un catalyseur (exemple:H2SO4),
on peut rendre l’estérification plus rapide, sans modifier l’équilibre
chimique.
L’expérience
montre que cette réaction est lente et athermique. Elle est limitée par la
réaction inverse appelée hydrolyse de l’ester qui se produit dans les mêmes
conditions. On aboutit à un équilibre chimique qui se traduit par une double
flèche. Le mélange réactionnel contient alors les quatre composes: acide,
alcool, ester et eau, dans des proportions bien définies, variables avec la
classe d’alcool. Par
élévation de température ou l’utilisation d’un catalyseur (exemple:H2SO4),
on peut rendre l’estérification plus rapide, sans modifier l’équilibre
chimique.