CORRIGES
EXERCICE I :
1. Nom, la formule semi-développée et la classe de chacun des deux isomères.
|
Nom |
Formule |
Classe |
|
Propan-1-ol |
CH3-CH2-CH2-OH |
I |
|
Propan-2-ol |
CH3-CHOH-CH3 |
II |
2. Nature, le nom et la formule semi-développée des produits chimiques formés
Lors de l’oxydation ménagée de ces deux alcools.
|
|
Nature |
Nom |
Formule |
|
I |
Aldéhyde |
Ethanal |
CH3-CH2-CHO |
|
II |
Cétone |
Ethanone |
CH3-CO-CH3 |
EXERCICE II :
1. formule brute : CxHyOz
![]() =
=![]()
%H=![]() =
=![]()
%O=![]() =
=![]()
Formule brute: C5H12O
2.
C2H5-CH(CH3)-CH2OH:
2-methylbutan-1-ol
EXERCICE III :
1. Composition massique de cet alcool.
mC=![]() x12=3,6g
x12=3,6g
%C=(mc/m)x100=3,6/6 x100=60
mH=7,2/18 x2=0,8g
%H=(mH/m) x100=![]() x100=13,33
x100=13,33
%O=100-(60+13,33)=26,67
2. Masse molaire.
%O=(16/100) x100 => M=1600/%O=1600/26,67=60g.mol-1.
3. formule brute
CnH2n+2 O
M=mC+mH+mO=12n+2n+2+16=14n+18=60 =>n=(60-18)/14=3
La formule brute est: C3H8O
4. Propan-2-ol
EXERCICE IV :
1- Cr2O-7/CH3CH2OH
2-3CH3CH2OH + 2Cr2O-7 +16H3O+ →3CH3COOH +4Cr2+ +27H2O
3-Nombre de moles apporté par le dichromate de potassium après dilution avec le sang:
M(K2Cr2O7)=2x39+2x52+7x16=294 g.mol-1
[Cr2O-7]initial =14,7 g/l =14,7/294=0,05 mol/l soit n(Cr2O-7)initial=0,05x0,020=0,001 mol
[Cr2O-7]final=0,024 mol/l soit n(Cr2O-7)final=0,024x0,030=0,00072 mol
Le nombre de mole de dichromate ayant réagi est:
nr= n(Cr2O-7)initial - n(Cr2O-7)final=0.001-0.00072=0,00028 mol.
Le nombre de moles d’alcool ayant réagi est:
n(alc)/3=n(Cr2O-7)/2 => n(alc)=1,5x0,00028=0,00042 moles //d’après l’équation-bilan
Tout l’alcool présent dans le sang initial a totalement réagi ;
[alc]=0,0042x46/0,01=1,93g/l
EXERCICE V:
A.
1-Formule semi-développée du glycérol (propane-1,2,3-triol).
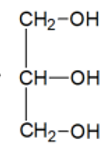
2-
Formule brute:
(C17H33COO)3C3H5
Formule semi-développée:
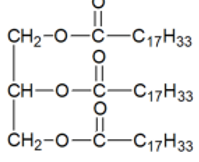
B.
1-.
Saponification
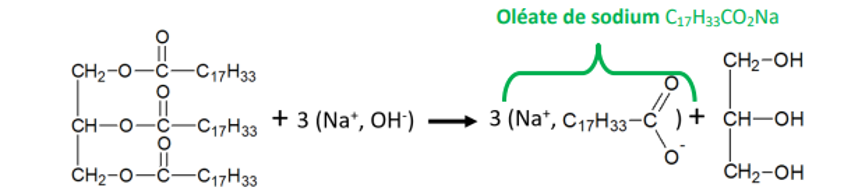
2-Masse de savon obtenue.