LE NOYAU ATOMIQUE
Structure d’un noyau atomique
Expérience de
Rutherford
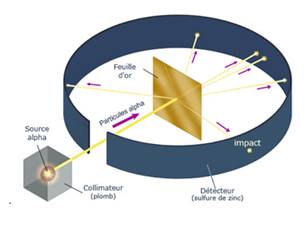
L’expérience consiste à placer sur le trajet d’un faisceau de particules une feuille d’or très mince (épaisseur de l’ordre du micromètre :1 m =10-6 m). Ces particules chargées d’électricité positive, sont émises dans le vide par une sources radioactive et canalisées grâce à des diaphragmes. Elles sont invisibles, mais sous leur impact, l’écran devient fluorescent, ce qui permet de suivre leur trajet depuis la sortie des diaphragmes jusqu’à leur arrivée sur l’écran.
Matériel utilisé :
-Source radioactive: un morceau de radium est placé dans une boîte de plomb percée d'un petit orifice, créant un faisceau étroit de particules alpha.
-Cible : une fine feuille d'or, choisie pour sa grande malléabilité qui permettait de la réduire à une épaisseur de l’ordre du micromètre.
-Détecteur : un écran fluorescent en sulfure de zinc, placé autour de la feuille d'or, qui produit de minuscules éclairs de lumière (scintillations) lorsqu'il est frappé par une particule alpha.
Observations :
-La plupart des particules alpha (99,9 %) traversent la feuille d'or sans subir de déviation, donc ne rencontre pas d'obstacle.
-Quelques particules sont déviées à des angles importants.
-Un très petit nombre de particules (environ 1 sur 8 000) rebondit carrément en arrière, comme si elles avaient heurté un obstacle dense.
Interprétation :
-Dans la feuille d'or et, par extension dans la matière, il existe de grands espaces vides. On dit que la matière est une structure lacunaire. Elle est faite en grande partie de vide.
-la déviation de certaines particules s'explique par la présence, dans la feuille d'or, de corpuscules chargés d'électricité positive, qui repoussent les particules passant à proximité. Ces particules sont appelées noyaux atomiques.
- La charge positive et la masse de l'atome sont concentrées dans un petit noyau.
Conclusion: un atome possède un noyau, chargé d'électricité positive, de dimensions très petites par rapport à l'atome.
Les constituants d’un noyau atomique
Le noyau est constitué des protons et des neutrons. On les appelle des nucléons.
-Le proton est chargé d’électricité positive.
Charge du proton : qp=e=1,6.10-19C
Masse du proton : mp=1,67.10-27kg
-Le neutron est électriquement neutre, il ne porte pas de charge électrique.
Charge du neutron : qn=0
Masse du neutron : mn=1,67.10-27kg
Les protons sont les seuls responsables de la charge positive du noyau.
Le modèle atomique de Rutherford
Suite à l’expérience ci-dessus, Rutherford propose une
structure atomique basée sur trois principes:
- Le noyau: Au centre de l’atome se trouve un noyau extrêmement petit, dense et charge positivement.
- Le vide; entre le noyau et les électrons, il n’y a rien. L’atome est essentiellement constitué du vide (structure lacunaire).
- Les électrons: Les électrons (chargés négativement et de masse négligeable) et gravitent autour du noyau un peu comme des planètes autour du soleil
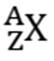
Représentation symbolique d’un noyau atomique
L’élément
est représenté :
A : nombre de
masse, il désigne le nombre de proton plus le nombre de neutrons.
Z : numéro
atomique ou nombre de charge, désigne le nombre de proton.
N : nombre de
neutron.
Donc, pour
un élément de numéro atomique Z et de nombre de masse A, nous aurons :
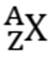
Remarque
:
· Dans un atome, le nombre d’électrons est égal au nombre de protons Z.
· Si l’élément est ionisé (chargé), le nombre d’électron est différent du nombre de proton
Exemple ; l’atome de sodium Na possède 11 protons et 11 électrons
L’ion sodium Na+ possède 11 protons et 10 électrons
Les isotopes
Les atomes qui ont le même numéro atomique Z, mais de nombre de masse A différents, sont des isotopes de l’élément de numéro atomique Z.
Exemple: ![]() et
et ![]() sont
les isotopes de l’uranium
sont
les isotopes de l’uranium
On appelle nucléide, l’ensemble des atomes dont le noyau possède le même nombre de charge et le même nombre de masse. Des nucléides isotopes appartiennent au même élément chimique.
EXERCICES
EXERCICE I :
1. L’atome d’oxygène possède 3
isotopes: ![]() ;
;![]()
![]()
Déterminer, pour chaque isotope, le nombre de charge Z, le nombre de masse A et le nombre de neutrons N.
2. L’uranium présente dans la nature deux isotopes : Uranium 235 et Uranium 238. Son noyau possède 92 protons.
21. Quel est le nombre de neutrons dans chaque isotope ?
22.Donner les représentations du noyau de l’atome d’uranium.
EXERCICE II :
On considère un atome de carbone dont le
noyau est représenté par ![]()
1. Déterminer la composition du noyau de cet atome
2. Combien d’électrons possède-il?
Ecrire sa formule électronique et sa représentation de Lewis
3. En utilisant la masse des particules donnée dans le cours, calculer :
-la masse du noyau
-la masse de l’atome
EXERCICE III :
1.L’atome de sodium possède 11 électrons. Ecrire sa configuration électronique
2. L’atome d’hélium a pour notation symbolique![]() .Ecrire sa configuration
électronique
.Ecrire sa configuration
électronique
3. L’atome d’Argon appartient à la 18ème colonne de la 3ème période. Ecrire sa configuration électronique
4. Le chlorure de sodium est composé des ions Cl- et Na+. Donner
la configuration électronique de ces deux ions.
Données : : ![]()
Avez-vous
un exercice à proposer au Forum ?
Cliquez-ici
Suivez-nous sur notre page Facebook
Merci de votre visite
Laissez un commentaire