ALCENES-ALCYNES
FORMULES GENERALES-NOMENCLATURE -ISOMERIE
Formules générales
Ø Les alcènes sont des hydrocarbures a chaine ouverte comportant une double liaison. Ils possèdent au moins deux atomes de carbone. A cause de la double liaison, un alcène possède deux atomes d’hydrogène de moins que l’alcane ayant le même nombre d’atomes de carbone.
La formule générale des alcènes est: CnH2n avec n≥2
Remarque:
CnH2n est aussi la formule générale des cyclanes qui sont des isomères d’alcènes.
Ø Les alcynes sont des hydrocarbures a chaine ouverte comportant une triple liaison. Un alcyne possède donc 2 atomes d’hydrogène de moins que l’alcène ayant le même nombre d’atome de carbone.
La formule générale des alcynes est: CnH2n-2
Remarque:
CnH2n-2 est aussi la formule générale des diènes, hydrocarbure a chaine ouverte possédant 2 doubles liaisons. Les diènes sont des isomères d’alcynes.
Structure des alcènes
Un exemple d’alcène: l’éthylène
L’éthylène C2H4 est un gaz dans les conditions normales de température et de pression. La molécule est plane et comporte une double liaison.
La formule développée peut s’écrire:
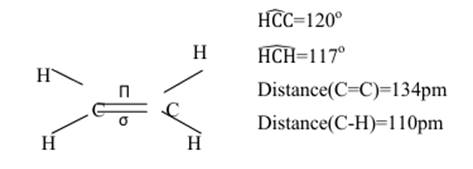
Les deux liaisons composant la liaison éthylénique ne sont pas équivalentes:
-l’une
solide, présentant une symétrie de révolution autour de l’axe C-C: c’est
la liaison sigma ![]() .
.
-l’autre,
beaucoup plus fragile et donc facile à rompre: c’est la liaison pi ![]()
Lorsqu’un atome de carbone est lie à 3 atomes
avec lesquels il échange 2 liaisons simples et une double, les angles entre les
liaisons valent 120![]() . On dit que le carbone
est trigonal, la double liaison entraine la rigidité de de la molécule;
la libre rotation est impossible autour de la liaison C-C.
. On dit que le carbone
est trigonal, la double liaison entraine la rigidité de de la molécule;
la libre rotation est impossible autour de la liaison C-C.
Structure des alcynes
Exemple d’alcyne : acétylène
L’acétylène C2H2 est un gaz dans les conditions normales de température et de pression. Les deux atomes de carbone établissent entre eux trois liaisons covalentes (liaison acétylénique).
La formule développée peut s’écrire:

Les trois liaisons ne sont pas équivalentes. Il
existe une liaison sigma ![]() solide et deux
liaisons pi
solide et deux
liaisons pi ![]() fragiles.
fragiles.
L’étude de la structure géométrique de la molécule montre que:
-la molécules est linéaire: les centres des 4 atomes sont alignés.
-la longueur de la triple liaison C≡C aut 120pm, donc inférieure à celle de la double liaison;
- la longueur des liaisons C-H vaut 110pm.
Lorsqu’un atome de carbone est lié à deux atomes par une simple et une triple liaison, les centres des trois atomes sont alignés: le carbone est digonal.
Nomenclature des alcènes et des alcynes
Le nom d’un alcène ou d’un alcyne s’obtient à partir du nom de l’alcane correspondant en remplaçant la terminaison ane de l’alcane respectivement par -éne ou -yne, précédée entre tiret de l’indice de position de la double ou triple liaison. La position de la double liaison ou celle de la triple liaison est indiquée par le numéro de l’atome de carbone doublement ou triplement lié, possédant l’indice le plus petit. La chaine principale est celle la plus longue contenant la double ou triple liaison.
Nomenclature des alcènes
Étapes de Nomenclature :
- Identifier la plus longue chaîne carbonée contenant la double liaison.
- Numéroter la chaîne principale :En partant de l'extrémité la plus proche de la double liaison (qui est en position 1).
- Identifier les substituants et leur position.
- Assembler le nom :indice-substituant + nom de la chaîne principale avec indice de la double liaison + suffixe -ène
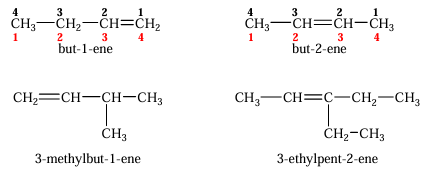
Nomenclature des alcynes
Étapes de Nomenclature :
- Identifier la plus longue chaîne carbonée contenant la triple liaison.
- Numéroter la chaîne principale :En partant de l'extrémité la plus proche de la triple liaison.
- Indiquer la position de la triple liaison et le suffixe :-1-yne.
- Assembler le nom :nom de la chaîne principale + indice de la triple liaison + suffixe -yne
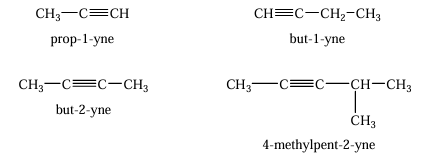
Isoméries
Ø Isomérie de constitution
-isomérie de position: les isomères ne diffèrent que par la position de la liaison multiple.
Exemples :
Isomères de position : le but-1-éne (CH2=CH-CH2-CH3) et le but-2-éne (CH3-CH=CH-CH3)
-isomères de chaine : les isomères ne diffèrent que par leur chaine carbonée.
Exemples :
Isomères de chaine. -Le but-1-éne (CH2=CH-CH2-CH3) et le 2-méthylprop-1-éne (CH3-C(CH3)=CH2 )
-le but-2-éne (CH3-CH=CH-CH3 ) et le 2-méthylprop-1-éne (CH3-C(CH3)=CH2 ).
Ø Stéréo-isomérie:
Les stéréo-isomères sont des isomères qui ne diffèrent que par l’agencement spatial des atomes. La stéréo-isomérie se rencontre chez les alcènes.
Si nous considérons le but-2-éne, la molécule peut se présenter dans l’espace sous deux formes appelées configurations
- Il existe deux isomères :
- Z-but-2-ène (Z de l’allemand Zusammen) : les groupes identiques (CH₃) sont du même côté de la double liaison.
- E-but-2-ène (E de l’allemand Entgegen) : les groupes identiques (CH₃) sont de côtés opposés.
|
CH₃ H \ / C = C / \ H CH₃
Z (cis)
|
CH₃ CH3 \ / C = C / \ H H
E (trans)
|
Remarques :
§ Les configurations Z/E sont appelées des diastéréoisomères,
§ L’isomérie Z/E était autrefois appelée isomérie Cis/trans. On rencontre parfois cette appellation lorsque les substituants des deux carbones doublement liés sont les mêmes.
PROPRIETES PHYSIQUES
Dans les conditions normales :
§ Les alcènes et les alcynes de C2 à C4 sont gazeux, de C5 à C18 les alcènes sont liquides alors que les alcynes eux sont liquides de C5 à C15. Les autres alcènes et alcynes sont solides.
§ Ces hydrocarbures ne sont généralement pas solubles dans l’eau ou le sont peu.
PROPRIETES CHIMIQUES
Combustion complète dans le dioxygène
Cas des alcènes : CnH2n + O2 → nCO2 + nH2O
Cas des alcynes : CnH2n-2 + O2 → nCO2 + (n-1) H2O
Réaction d’addition
Une réaction d’addition est une réaction chimique au cours de laquelle deux réactifs s’unissent pour former un seul produit, sans perte d’atome.
Elle concerne généralement les molécules possédant une double liaison (comme les alcènes) ou une triple liaison. Les liaisons pi sont fragiles et peuvent se rompre facilement.Lorsqu’une liaison pi s’ouvre, chaque atome de carbone dispose d’un électron célibataire qu’il peut engager dans une liaison avec un autre atome.
Caractéristiques :
- Un seul produit final.
- Pas de sous-produits.
- Typique des réactions sur des liaisons multiples.
Hydrogénation
L’hydrogénation d’un alcène nécessite l’utilisation d’un catalyseur: le nickel et le palladium.
Cas des alcènes
En présence du nickel, l’éthylène réagit avec le dihydrogène pour donner de l’éthane.
Exemple:
CH2 = CH2 + H2 → CH3─ CH3
Au cours de cette réaction, il y a eu ouverture de la liaison π. Chaque atome de carbone a engagé son électron célibataire disponible dans une liaison avec un atome d’hydrogène.
Cas des alcynes
- l’hydrogénation de l’acétylène conduit à l’éthylène en présence du palladium (Pd),
Exemple:
![]()
-Avec le nickel, la réaction se poursuit et conduit à l’éthane
![]()
L’hydrogénation d’un alcyne conduit à un alcane, il faut 2 molécules de dihydrogène.
En général, l’hydrogénation d’un alcyne conduit à un alcène (hydrogénation incomplète) et à un alcane (hydrogénation complète). Les équations-bilans générales de l’hydrogénation des alcynes s’écrivent :
CnH2n-2 + H2 → CnH2n
CnH2n-2 + 2H2 → CnH2n+2
En présence du palladium, la réaction s’arrête au stade d’alcène.
Halogénation
L’addition d’un halogène sur un alcène lorsqu’elle est possible donne un alcane dihalogéné et sur un alcyne lorsque la réaction est possible se fait avec fixation d’une molécule de X2 (X=Cl, Br,…).
Addition du dichlore sur l’éthylène
CH2= CH2 + Cl2 → CH2Cl= CH2Cl (1,2-dichlorométhane)
On obtient un liquide huileux, le 1,2-dichlorométhane.
Cette réaction, appelée la chloruration est, comme l’hydrogénation, une réaction d’addition qui s’accompagne d’un profond changement de structure.
Addition du dibrome sur l’éthylène
On obtient du 1,2-dibromoethane, CH2Br-CH2Br
Hydratation
Cas des alcènes :
L’action de l’eau sur les alcènes est généralement possible à haute température, en présence du catalyseur l’acide sulfurique. Elle conduit à la formation d’un alcool.
CH2= CH2 + H2O →CH3-CH2OH
CH3-CH2-CH=CH2 + H2O CH3-CH2-CH2-CH2OH ou CH3-CH2-CHOH-CH3
Remarque :
Dans le premier exemple où l’alcène est symétrique, on obtient un seul produit et dans le second cas où l’alcène est dissymétrique, l’hydratation conduit à deux produits dont l’un est majoritaire et l’autre minoritaire.
Règle de Markovnikov : Lors de l’addition de HO-H sur un alcène dissymétrique, l’atome d’hydrogène se fixe sur l’atome de carbone le plus hydrogéné (moins substitué)
Cas des alcynes
En présence de l’ion mercure (Hg2+), l’addition de l’eau sur un alcyne conduit à une cétone et dans un cas particulier de l’acétylène à un aldéhyde.
CH≡C-CH3 + H2O ⎯⎯ CH3-CO-CH3 (propanone)
CH≡CH + H2O ⎯⎯ CH3-CHO (éthanal)
Comme l’addition d’eau sur un alcène, celle d’un alcyne aussi suit aussi la règle de Markovnikov.
Addition d’un hydracide halogéné : H-X
L’addition d’un hydracide halogéné H-X (X=Cl, Br,…) sur un alcène ou un alcyne se fait par fixation d’une molécule sur la double ou triple liaison.
Cas des alcènes
L’addition de chlorure d’hydrogène sur l’éthylène conduit au chlorométhane.
CH2=CH2 + HCl → CH3-CHCl
Cette réaction se produit avec les autres alcènes.
CH3-CH=CH2 + HCl → CH3-CHCl-CH3 ou CH3 -CH2-CH2Cl
L’expérience montre qu’on obtient principalement le 2-chloropropane dans lequel l’hydrogène s’est fixé sur le carbone le plus hydrogéné.
Cas des alcynes
Dans le cas d’un alcyne on peut avoir fixation de deux molécules de HCl.
CH≡C-CH3 + HCl → CH2=CCl-CH3 ou CHCl=CH-CH3
CH≡C-CH3 + 2HCl → CH3-CCl2-CH3 ou CH2Cl-CHCl-CH3
Réaction de polymérisation
C’est l’addition répétée (polyaddition) d’un très grand nombre de molécules insaturées identiques (monomères). Elle conduit à une macromolécule (polymère). Le monomère doit contenir au moins une liaison C=C.
Polymérisation de l’éthylène
n(CH2=CH2) → (-CH2-CH2-)n : Polyéthylène où n est le degré de polymérisation,
-CH2-CH2- : le motif
Les polyéthylènes sont des thermoplastiques: ils deviennent fluides lorsqu’on les chauffe, ce qui permet de leur donner une forme.
Selon les conditions expérimentales, on obtient:
-le polyéthylène basse densité obtenu à haute pression utilise pour fabriquer des emballages souples (sachets d’emballage, bouteilles, isolants électriques…)
- le polyéthylène basse densité obtenu à pression peu élevée utilise pour fabriquer des casiers, des futs, des jouets
Polymérisation du chlorure de vinyle
Le chlorure de vinyl CH2=CHCl possède une double liaison, comme l’éthylène. Il se polymérise en donnant le Polychlorure de vinyl (PCV).
n(CH2=CHCl) → (-CH2-CHCl-) Polychlorure de vinyl (PCV)
L'équation de polymérisation du chlorure de vinyle (aussi appelé chloroéthène) est une réaction d’addition de plusieurs molécules de monomère de chlorure de vinyle pour former le polychlorure de vinyle (PVC).
Équation générale :
n CH₂=CHCl → [–CH₂–CHCl–]ₙ
- CH₂=CHCl : chlorure de vinyle (monomère),
- [–CH₂–CHCl–]ₙ : polychlorure de vinyle (polymère),
- n : nombre de molécules (grand nombre)
Polymérisation du styrène
Le styrène se polymérise pour donner le polystyrène. Sous sa forme expansée, il est utilisé dans l’emballage des objets fragiles.
L’équation de la polymérisation du styrène est la transformation de molécules de styrène (monomères) en polystyrène (polymère).
Équation générale :
n C₆H₅-CH=CH₂ → [–CH₂–CH(C₆H₅)–]ₙ
- C₆H₅-CH=CH₂ : formule du styrène (ou phényléthène),
- [–CH₂–CH(C₆H₅)–]ₙ : structure répétitive du polystyrène,
- n : nombre de monomères
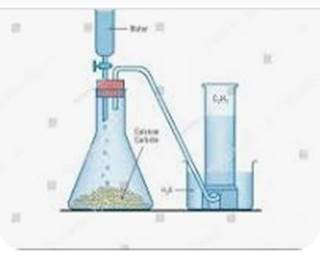
PREPARATION DE L’ACETYLENE AU LABORATOIRE
L’acétylène est obtenu au laboratoire par action de l’eau sur le carbure de calcium (C2Ca).
L’équation-bilan de la réaction s’écrit:
CaC2 + 2H2O→C2H2 + Ca(OH)2
EXERCICES
EXERCICE I: nommer les hydrocarbures suivants, et donner leurs formules brutes
1.
![]()
2.
![]()
3.
![]()
4.
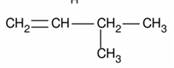
5.
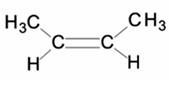
EXERCICE II : écrire les formules semi-développées des hydrocarbures suivants:
1. but-1-yne
2. pent-1-yne
3. pent-2-yne
4. 3-chloro-5-isopropyl-3-méthyloct-1-yne
5. 4-éthylhex-2-yne
EXERCICE III
SoitAun hydrocarbure aliphatique insaturé, de masse molaireM=68g⋅mol−1, dont la chaine carbonée renferme une triple liaison.
a) Trouver la formule brute de l'hydrocarbureA.
b) trouver tous les isomères possibles deAet les nommer.
On donne :
M(H)=1g⋅mol−1etM(C)=12g⋅mol−1
EXERCICE IV:
On réalise la chloration d’un alcène A dans une industrie chimique. Le produit B obtenu a une masse molaire égale à 113g/mol. Un élève veut établir la formule brute du produit B et celle de l’alcène A. Il éprouve des difficultés. Viens-lui-en aide pour répondre aux questions suivantes.
1- Ecris l’équation bilan générale de la chloration des alcènes.
2- Exprime la masse molaire de B en fonction de n (nombre d’atomes de carbone de A et B)
3- Trouve le nombre d’atones de carbone n.
4- Etablis la formule brute de B et celle de A.
On donne : M (H) = 1g/mol; M(C) = 12g/mol; M (Cl) = 35,5g/mol.
EXERCICE V:
1 Donner la formule brute d’un alcyne dont la molécule renferme n atomes de carbone. Exprimer en fonction de n le pourcentage en masse de l’élément d’hydrogène (%H).
2. L’analyse de 4,5g de l’alcyne montre qu’il renferme 0,45g d’hydrogène. En déduire sa formule moléculaire A, ainsi que sa formule semi-développée et son nom.
3. On lui additionne du dichlore, on obtient un dérivé saturé B. Ecrire son équation-bilan en précisant la formule semi-développée et le nom du composé B.
4. On fait barboter l’alcyne précédent dans l’eau (H2O) à 700 C en présence de l’oxyde de mercure II (HgO) et de l’acide sulfurique. On obtient un composé organique C contenant un atome d’oxygène appelé composé carbonylé.
4.1. Ecrire l’équation-bilan de la réaction.
4.2. Donner la famille à laquelle appartient ce composé carbonylé.
5. Donner le nom de l’alcène D qui dérive de A, ainsi que son équation-bilan.
6. Ecrire l’équation-bilan de la réaction d’hydratation de D.
7. Ecrire l’équation-bilan de la réaction de polymérisation de cet alcène en nommant le(s) produit(s) et le(s) réactif(s).
EXERCICE VI:
Un hydrocarbureAcontient en masse6fois plus de carbone que d'hydrogène.
1) a) Déterminer la formule brute générale de cet hydrocarbure.
b) A quelle(s) famille(s) d'hydrocarbure appartient-il ?
c) Écrire les formules semi-développées possible deAsachant queArenferme8atomes d'hydrogène.
2) La chaine carbonée de l'hydrocarbureAest linéaire ; de plusApossède des stéréo-isomèreZ/E.
Représenter ces stéréo-isomères.
3) Le craquage deAdans un vapocraqueur conduit à la formation de l'éthylène.
a) Toute la quantité deAn'a pas été transformée, déterminer la composition centésimale molaire du mélange gazeux du vapocraqueur à la fin de la réaction sachant que sa densité par rapport à l'air estd=1.2068.
b) Après refroidissement du mélange, on y ajoute du dichlore ; puis on place le nouveau mélange à l'obscurité.
Écrire les formules semi-développées et les noms des produitsBetCformés.
Bétant le produit issu de l'action du dichlore surA.
c) Le chauffage des produitsBetCprovoque l'élimination d'une molécule de chlorure d'hydrogèneHCl.
Le composéCdonne le composéDet le chlorure d'hydrogène.
EXERCICE VII:
1) Un hydrocarbure aliphatique saturé(A)a une masse molaire moléculaireM=58g⋅mol−1.
a) Trouver la formule brute de(A)
b) Écrire les formules semi-développées possibles et donner le nom des différents isomères de(A).
c) Identifier l'isomère(A1)de(A)sachant qu'il présente une chaine ramifiée.
2) l'action du dibromeBr2sur l'hydrocarbure(A1)en présence de la lumière, donne un mélange de dérivés bromés dont l'un est un dérivé dibromé noté(B)
a) Écrire l'équation chimique de la réaction conduisant à la formation de(B)en utilisant les formules brutes.
b) Donner toutes les formules semi-développées possibles de(B)et le nom des isomères correspondants
c) La structures de l'hydrocarbure de départ(A1)a-t-elle été modifiée au cours de cette réaction.
3) L'un des isomères(B1)de(B)peut être obtenu par une réaction d'addition du dibrome sur un alcène.
a) Trouver la formule brute de cet alcène.
b) Écrire la formule semi développée et le nom de cet alcène.
c. Écrire l'équation de la réaction d'addition en utilisant les formules brutes.
d) la structure de l'hydrocarbure de départ a-t-elle été modifiée au cours de cette réaction ?
<Avez-vous
un exercice à proposer au Forum ?
Cliquez-ici
Merci de votre visite
Laissez un commentaire