CORRIGES
EXERCICE I: nommer les hydrocarbures suivants, et donner leurs formules brutes
1.
Nom : 2-methylprop-1-ene
Formule brute : C4H8
2.
Nom : but-2-ene
Formule brute : C4H8
3.
Nom : 3-méthylbut-1-yne
Formule brute : C5H8
4.
Nom: 3-methylbut-1-ene
Formule brute :C5H11
5.
Nom: (Z)-but-2-ene
Formule brute :C4H8
EXERCICE II :
1. CH2=CH-CH2CH3
2.
![]()
3.
![]()
4.
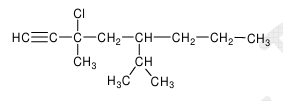
5.
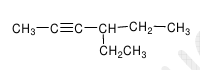
EXERCICE III
a) formule brute de l'hydrocarbureA.
CnH2n-2
M=12n+2n-2=14n-2=68 =>n=70/14=>n=5
A: C5H8
b) isomères possibles deAet les nommer.
![]() pent-1-yne
pent-1-yne
![]() pent-2-yne
pent-2-yne
EXERCICE IV:
1- Equation bilan générale CnH2n + Cl2 → CnH2nCl2
2- J’exprime la masse molaire de B en fonction de n. A a pour formule brute : CnH2n
B résulte de l’addition du dichlore Cl2 sur A ; il a donc pour formule : CnH2nCl2
M (B) = M (CnH2nCl2) =14n+71
3- Je trouve le nombre d’atones de carbone n.
113= 12n + (1x2n) + (35,5x2) 113=14n +71; 14n = 42
14n = 42 ; n=42 14 ; n= 3
4- J’établis la formule brute de B et celle de A.
n= 3;
B: C3H6Cl2;
A: C3H6
EXERCICE V:
1. Alcyne A: CnH2n-2
M(A)=12n +2n-2=14n-2
M(H)=2n-2
![]()
![]() =
=![]()
Formule de A :C3H4, nom: propyne, FSD: CH3-C≡CH
3. CH3-C≡CH + 2Cl → CH3-C(Cl2)-CHCl2 (B)
(B): 1,1-dichloro-2,2-dichloropropane
4.1. CH3-C≡CH3 + H2O → CH3-CO-CH3 (C): propanone
4.2. Ce composé appartient à la famille des cétones
5. CH3-C≡CH3 + H2 → CH3-CH=CH2 (D): propéne
6. CH3-CH=CH2 + H2O CH3CH(OH)-CH3: propan-2-ol CH3-CH2-CH2OH: propan-1-ol
7. n(CH3-CH=CH2) → (-CH-CH-)n: polypropéne
EXERCICE VI:
1) a) formule brute générale de cet hydrocarbure.
Formule: CxHy avec mC=6mH
Soit la formule brute : CₓHᵧ
- Masse du carbone = 12x
- Masse de l’hydrogène = y
On dit :
> Masse du carbone = 6 × Masse de l’hydrogène
Donc :
12x = 6y
⇒ x = n =>y=2n
formule brute générale : CₙH₂ₙ
b) A quelle(s) famille(s) d'hydrocarbure appartient-il ?
- des alcènes (hydrocarbures avec une double liaison)
- ou des cycloalcanes (hydrocarbures cycliques saturés)
c) Écrire les formules semi-développées possible deAsachant queArenferme8atomes d'hydrogène.
Ce composé peut être :
· Un alcène (double liaison, chaîne ouverte) :
- but-1-ène : CH₂=CH–CH₂–CH₃
- but-2-ène : CH₃–CH=CH–CH₃
- cis-but-2-ène et trans-but-2-ène (isomères géométriques)
· Un cycloalcane (cycle saturé) :
- cyclobutane : un cycle de 4 carbones
- méthylcyclopropane : un cycle de 3 carbones + 1 ramification CH₃
2) La chaine carbonée de l'hydrocarbureAest linéaire ; de plusApossède des stéréo-isomèreZ/E.
- C’est un alcène (présence d’une double liaison C=C)
- Chaque carbone de la double liaison porte deux groupes différents, condition nécessaire à l’existence de stéréo-isomères géométriques (Z/E)
L'hydrocarbure A est donc but-2-ène : CH₃–CH=CH–CH₃
Représentations des stéréo-isomères :
· Isomère Z (zusammen = ensemble)
Les deux groupes identiques (CH₃) sont du même côté de la double liaison.
CH3 CH3
\ /
C = C
/ \
H H Z-but-2-ène :
· Isomère E (entgegen = opposé)
Les deux groupes CH₃ sont de côtés opposés.
CH3 H
\ /
C = C
/ \
H CH3 E-but-2-ène
3) Le craquage deAdans un vapocraqueur conduit à la formation de l'éthylène.
Le craquage du but-2-ène peut être schématisé par :
C₄H₈ → C₂H₄ + C₂H₄
(1 mol de C₄H₈ donne 2 moles d’éthylène)
a) Pour déterminer la composition centésimale molaire du mélange gazeux final (après craquage partiel de A en éthylène), on utilise la densité par rapport à l’air.
M_mélange = d × M_air = 1,2068 × 29 ≈ 35 g/mol
Hypothèse de craquage
On suppose :
- n mols de C₄H₈ initialement
- x mols ont été craqués → il reste n – x mols de C₄H₈
- 2x mols de C₂H₄ produits
→ Total de mols : (n – x) + 2x = n + x
Masse molaire moyenne
M_mélange = (n–x)×M(C₄H₈) + 2x×M(C₂H₄) / (n + x)
- M(C₄H₈) = 56 g/mol
- M(C₂H4)=28g /mol
M_mélange = [(n–x)×56 + 2x×28] / (n + x)
35=[56n-56x+56x]/(n+x)
35=56n/(n+x)
Pour n=1 mol
x=0,6 mols
Restant de C₄H₈:0,4 mol
C₂H₄ formé: 1,2 mols
Total:1,6 mol
→ Pourcentage molaire :
- C₄H₈ : (0,4 / 1,6) × 100 = 25%
- C₂H₄ : (1,2 / 1,6) × 100 = 75%
b)
Bétant le produit issu de l'action du dichlore surA.
Puisque A est un alcène de chaîne linéaire avec 8 hydrogènes et qu'il présente des isomères Z/E, il s'agit probablement de but-2-ène (C4H8).
Réaction de A avec Cl₂ à l'obscurité
Quand on ajoute du dichlore (Cl₂) à un alcène en absence de lumière :
- Il n’y a pas de substitution radicalaire
- Il se produit une addition électrophile : les deux atomes de chlore s’ajoutent sur la double liaison.
Réaction de Cl₂ sur le but-2-ène (A)
Formule semi-développée de A :
CH₃–CH=CH–CH₃ (but-2-ène)
Réaction :
CH₃–CH=CH–CH₃ + Cl₂ → CH₃–CHCl–CHCl–CH₃
Produit B :
- Nom : 2,3-dichlorobutane
- Formule semi-développée : CH₃–CHCl–CHCl–CH₃
Produit C: CH2Cl-CH2Cl
c) Le chauffage des produitsBetCprovoque l'élimination d'une molécule de chlorure d'hydrogèneHCl.
Le composéCdonne le composéDet le chlorure d'hydrogène.
Lorsqu’on chauffe les produits B et C (2,3-dichlorobutane), il peut se produire une élimination de HCl, typique d’une réaction d’élimination de type E2, qui régénère une double liaison (formation d’un alcène).
Réaction d’élimination sur C
C : 2,3-dichlorobutane :
CH₃–CHCl–CHCl–CH₃
Élimination de HCl → perte d’un H sur un carbone et d’un Cl sur l’autre → formation d’une double liaison entre C2 et C3.
Produit D obtenu :
CH₃–CH=CH–CH₃
Donc : D = but-2-ène, l’alcène de départ (rétro-élimination).
Bilan de la réaction :
C (2,3-dichlorobutane) → D (but-2-ène) + HCl
Cela montre que la réaction d’addition Cl₂ sur l’alcène est réversible par chauffage (élimination)
EXERCICE VII:
1) Un hydrocarbure aliphatique saturé(A)a une masse molaire moléculaireM=58g⋅mol−1.
a) formule brute de(A)
CnH2n+2
M=12n+2n+2=14n+2=58 =>n=56/14=4
Formule brute de(A): C4H10
b) formules semi-développées possibles et noms des différents isomères de(A).

c) l'isomère(A1)de(A)qui présente une chaine ramifiée.
A1:
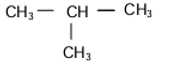
L’hydrocarbure (A1) est le 2-méthylpropane
2)
a) Réaction avec le dibrome (Br₂) en présence de lumière :
→ Il s'agit d’une réaction de substitution radicalaire (halogénation) sur un alcane ramifié, sous l’effet des UV.
Le Br₂ remplace deux atomes d’hydrogène pour donner un dérivé dibromé (B).
Formule brute de la réaction :
C4H10 + Br2 → C4H8Br2 + H2
Cela représente la formation d’un dibromo-dérivé à partir de 2-méthylpropane, avec élimination de 2 atomes d’hydrogène (remplacés par 2 Br).
Exemple de dérivé possible (B) :
Un des produits est : 1,2-dibromo-2-méthylpropane
b) Donner toutes les formules semi-développées possibles de(B)et le nom des isomères correspondants
À partir du 2-méthylpropane (C4H10), on peut former plusieurs dérivés dibromés notés (B) par substitution de deux atomes d'hydrogène par deux atomes de Br en présence de lumière (halogénation radicalaire).
Formule du 2-méthylpropane :
CH3
|
CH3 – CH – CH3
On identifie les positions où les hydrogènes peuvent être substitués par des Br :
- Carbone central (tertiaire) → 1 H
- Carbones terminaux (méthyle) → 6 H (3 sur chaque CH3)
Formules semi-développées possibles de (B) :
CH3–C(Br)(CH3)–CH2Br → Nom : 1-bromo-2-bromo-2-méthylpropane
CH3–C(Br2)(CH3)–CH3 → Nom : 2,2-dibromo-2-méthylpropane
(2 Br sur le même carbone central)
BrCH2–C(CH3)2–CH3 → Nom : 1-bromo-2-méthylpropane-2-yl bromide (forme équivalente au 1er isomère)
c)
Oui, la structure de l'hydrocarbure de départ (A1), qui est le 2-méthylpropane (C4H10), a été modifiée au cours de la réaction.
Explication :
- La réaction avec le dibrome (Br2) en présence de lumière est une substitution radicalaire.
- Elle remplace un ou plusieurs atomes d'hydrogène de la molécule par des atomes de brome.
- Le squelette carboné reste le même (la chaîne carbonée n’est pas rompue ni réorganisée), mais la nature des atomes liés au squelette change, ce qui modifie la structure chimique de la molécule.
Donc :
- Structure globale (chaîne) : inchangée
- Structure moléculaire (liaisons et atomes présents) : modifiée
3) a)
Pour obtenir l’isomère dibromé (B1) à partir d’une réaction d’addition du dibrome (Br₂) sur un alcène, il faut identifier un alcène qui possède le même squelette carboné que l’hydrocarbure de départ (A1), le 2-méthylpropane, et qui peut donner un dérivé dibromé isomère de (B).
Étape 1 : Trouver la formule brute du composé (B1)
L’hydrocarbure (A1) est le 2-méthylpropane : (CH₃)₂CH–CH₃, soit de formule brute C₄H₁₀.
Si on remplace deux atomes d'hydrogène par deux atomes de brome, on obtient un dibromo-dérivé de formule brute : C₄H₈Br₂.
Étape 2 : Rechercher un alcène correspondant
La réaction d'addition de Br₂ sur un alcène suit :
Alcène + Br₂ → dibromoalcane
On cherche donc un alcène de formule brute : C₄H₈.
Un alcène compatible est le 2-méthylpropène :
Formule semi-développée :
CH₂=C(CH₃)–CH₃
Nom : 2-méthylpropène
Formule brute : C₄H₈
Réaction :
CH₂=C(CH₃)–CH₃ + Br₂ → BrCH₂–CBr(CH₃)–CH₃ → (B1)
Conclusion :
b) L’alcène dont l’addition de Br₂ permet d’obtenir l’isomère dibromé (B1) est :
➡ Le 2-méthylpropène
➡ Formule brute : C₄H₈
➡ Nom : 2-méthylpropène
c. Voici l'équation de la réaction d'addition du dibrome (Br₂) sur le 2-méthylpropène (C₄H₈) :
C₄H₈ + Br₂ → C₄H₈Br₂
Avec les formules semi-développées :
CH₂=C(CH₃)–CH₃ + Br₂ → CH₂Br–CH(Br)(CH₃)–CH₃
Nom du produit : 1,2-dibromo-2-méthylpropane
Il s'agit d'une addition électrophile classique sur une double liaison C=C, le Br₂ se fixe sur les deux atomes de carbone initialement engagés dans la double liaison.
d) Oui, la structure de l'hydrocarbure de départ C₄H₁₀ (butane ou isobutane) a été modifiée au cours de cette réaction
Explication :
La réaction avec le dibrome (Br₂) en présence de lumière (hv) est une réaction de substitution radicalaire.
Dans cette réaction :
- Un atome d'hydrogène de C₄H₁₀ est remplacé par un atome de brome.
- Cela donne des composés comme C₄H₉Br ou des dérivés di-substitués C₄H₈Br₂.
Donc :
- Le nombre d'atomes de carbone reste le même (la chaîne carbonée n'est pas rompue).
- Mais la nature chimique de la molécule change : ce n’est plus un alcane pur, mais un halogénoalcane.
Conclusion :
Oui, la structure chimique de l’hydrocarbure C₄H₁₀ a été modifiée, car un ou plusieurs atomes d'hydrogène ont été remplacés par des atomes de brome