PILES ET ACCUMULATEURS
Piles
Description
et principe de fonctionnement d’une pile.
La pile
est un ensemble constitué d’électrolyte en contact avec deux électrodes de
nature différentes. Lorsque la pile fonctionne, elle est le siège d’un ensemble
de réaction chimique qui libère de l’énergie.
La pile
transforme cette énergie chimique en énergie électrique: On dit qu’elle
est un générateur électrochimique de courant continu.
Etude de quelques piles :
Exemple
de la pile Volta.
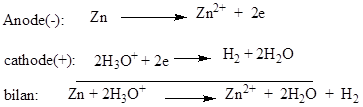
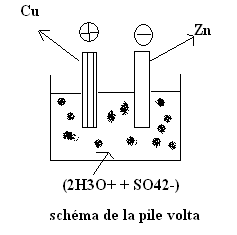
La f.é.m. de la pile volta est E≈1V.
NB:
Le courant électrique est dû au mouvement d’ensemble
des électrons de l’électrode de zinc vers celle de cuivre.
On l’appelle pile polarisable car une partie de
dihydrogène produit au pôle positif de la pile forme une gaine autour de
l’électrode de cuivre, ce qui augmente la résistance de la pile entrainant une
diminution de l’intensité du courant.
Pile
à dépolarisant: Exemple de la pile Leclanché.
Description
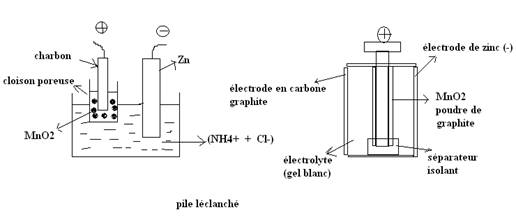
NB: le MnO2 est le dépolarisant (il
empêche la pile de se dépolariser).
La pile Leclanché est une pile saline, elle est aussi
dite pile sèche car l’électrolyte ne coule pas.
Fonctionnement
Lorsque la pile débite, les équations aux électrodes
sont:
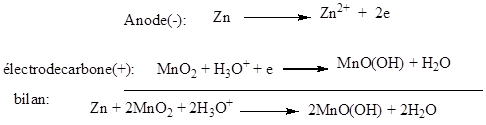
Le dépolarisant favorise un courant de longue durée,
la pile cesse de fonctionner dès qu’il y a manque de
zinc ou de MnO2.
Une
pile impolarisable: Exemple de la pile Daniell.
Description
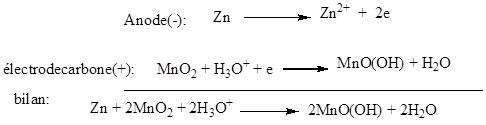
Fonctionnement
Les réactions aux électrodes sont:
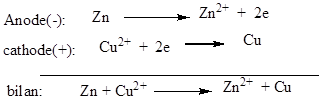
La f.é.m. est E ≈1,08V.
La solution s’appauvrie en Cu2+. Pour
maintenir la saturation de la solution en solution en Cu2+, on
dépose au fond du vase poreux des cristaux de sulfate de cuivre.
La
pile alcaline.
Description
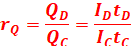
Fonctionnement
Cette pile fonctionne de la même façon que la pile
Leclanché. Son électrode négative étant constituée de zinc et celle positive,
de MnO2. Sa f.é.m. est de 1,5V.
Les piles alcalines ont un pouvoir énergétique plus
élevé et une grande capacité.
Les
accumulateurs.
Définition.
Un accumulateur
est un dispositif capable de stoker de l’énergie électrique sous forme chimique
et de la restituer, que l’appareil soit connecté ou non au secteur.
Une batterie d’accumulateur est un générateur
électrochimique déchargeable.
Fonctionnement
Un accumulateur fonctionne en charge ou en décharge.
Pour charger un accumulateur, on le branche aux bornes d’un dipôle actif.
Pendant la charge ou polarisation, l’accumulateur
fonctionne en récepteur. Il transforme l’énergie électrique reçue en énergie
chimique.
Pendant la décharge, ou dépolarisation, l’accumulateur
fonctionne en générateur, il transforme l’énergie chimique en énergie
électrique.
Les
caractéristiques électriques d’un accumulateur:
-
la
force électromotrice: Elle est indiquée en volt sur l’accumulateur.
-
La
capacité: c’est la quantité d’électricité que l’accumulateur peut fournir
au cours de la décharge. Elle s’exprime généralement en ampère-heure (Ah) et
1Ah = 3600C.
Le
rendement en quantité d’électricité.
La quantité
d’électricité consommée au cours de la charge pendant le temps tC sous un courant IC est:
QC=ICtC
La quantité
d’électricité fournie à la décharge pendant le temps tD
sous un courant ID est:
QD=IDtD
Le rendement en
quantité est le rapport de la quantité d’électricité QD au cours de
la décharge par la quantité d’électricité QC qui traverse
l’accumulateur au cours de la charge:
![]()
Le
rendement en énergie.
Comme la
résistance est très faible, l’effet joule est négligeable et l’énergie
consommée a la charge se réduit pratiquement à celle transformée en énergie
chimique:
WC=ECQC
Quant à l’énergie électrique fournie pendant la
décharge:
WD=EDQD
Le rendement de l‘énergie électrique WD
fournie au cours de la décharge à l’énergie électrique WC consommée
au cours de la charge.
![]()
NB:
On appelle cyclabilité, le
nombre de cycle «charges-décharges» qu’un accumulateur peut
effectuer.
Quelques
types d’accumulateurs.
L’accumulateur
au plomb.
Ø A la décharge, il se produit les réactions:
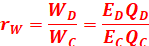
La f.é.m. de chaque
élément est de 2V.
Remarque:
Lorsque la décharge de l’accumulateur est importante,
l’augmentation de la concentration en ions pb2+peut conduire à la
formation d’un précipité de sulfate de plomb tel que:
![]()
Ø A la charge: Les réactions s’inversent au niveau
des électrodes.
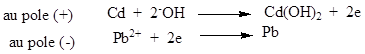
La f.c.é.m. des éléments est E’ = 2,2V
Accumulateur
cadmium-nickel.
Ø A la décharge, on a:
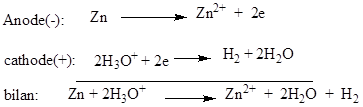
La f.é.m. d’un élément d’accumulateur cadmium-nickel
est de 1,3V.
Pendant la charge, les réactions ci-dessus
s’inversent.
EXERCICES
EXERCICE I:
Un voltmètre très résistant branché entre les bornes
d’une batterie de 10 éléments d’accumulateurs identiques associés en série,
indique 20 V en circuit ouvert et 19,8 V quand la batterie débite dans un
résistor de résistance 9,9 Ω.
1. Calculer la fem et la résistance interne de chaque élément.
2. Quelle serait l’intensité du courant si l’on court-circuitait les
deux bornes de la batterie par un résistor de résistance négligeable?
EXERCICE II:
Un accumulateur présente en charge une fcem moyenne de 2,2 V; sa charge demande un courant
de 2 A pendant 20 heures; sachant que cet accumulateur débite dans un
courant de décharge les 8/10 de la quantité d’électricité qui l’a traversé
pendant la charge et que la valeur moyenne de sa fem pendant la décharge est
1,9 V. Calculer:
1.Sa capacite.
2.L’energie électrique transformée en énergie chimique pendant la
charge.
3.L’energie chimique rendue pendant la décharge.
4.L’intensite du courant de décharge (suppose constant) quand celui-ci
s’effectue en 10 heures.
5.Le rendement en énergie.
EXERCICE III:
1.Un générateur de fem égale a
46 V et de résistance 1,5Ω sert a
charger une batterie de 20 éléments d’accumulateurs, mis en série, ayant chacun
une fcem constante égale a 2 V et une résistance interne de 0,05 Ω. On
néglige la résistance des fils de jonction.
Calculer l’intensité du courant dans le circuit.
2.Conservant le montage du 1, on dispose entre les bornes de la
batterie un résistor variable R. pour une certaine valeur R1 du
résistor, la ddp aux bornes de la batterie est 45,5
V. quelles sont les intensités des courants qui parcourent: le
générateurs, la batterie, la résistance?
Préciser la valeur R1 du résistor R.
EXERCICE IV:
Une
batterie d’accumulateur au plomb est chargée de 40 Ah.
1. La batterie se
décharge complètement en 1 h. La tension au cours de cette décharge est 11,8 V.
Quelle est l’énergie électrique fournie ?
2. On utilise la batterie pour démarrer une
automobile pendant 1,5 s. La batterie est alors traversée par un courant
d’intensité 0,2 kA et la tension à ses bornes est de 10,2V.
(a) Quelle est l’énergie
électrique fournie ?
(b) Quelle est la puissance
électrique ?
EXERCICE IV:
Un accumulateur au plomb (batterie de voiture) peut
être schématisé par une électrode de plomb et une électrode inerte recouverte
de dioxyde de plomb plongées dans une même solution contenant de l’acide
sulfurique et du sulfate de plomb.
1.Ecrire les deux demi-équations redox ainsi que la réaction naturelle
de la pile. E0Pb2+/Pb= - 0.13V et E0PbO2/Pb2+=
1.45V.
2.Quelle est la force électromotrice de cette pile en conditions standards?
3.Sachant qu’on est en solution aqueuse et en milieu acide, montrer que
PbO2et Pb sont consommés par des réactions parasites même
lorsque l’accumulateur est en circuit ouvert. E0O2/H2O=
1.23V et E0H+/H2= 0.00V.
4.Cette batterieaune capacité de 133 Ah et elle est
employée sous une intensité de 90A pour le démarrage de la voiture. Quelle
masse minimum de dioxyde de plomb doit-elle contenir?
MPb= 207 g.mol-1et
MO=16g.mol-1.
Avez-vous
un exercice à proposer au Forum?Cliquez-ici
Merci de votre visite
Laissez un commentaire