CORRIGES
EXERCICE I:
1. En circuit ouvert, I=0, U=E=20 <= >nE1=20=>E1=20/10=2 V.
Quand la batterie débite dans un résistor, U=E1-(R+r)I
2. Si on court-circuite les deux bornes de la batterie, U=0
U=E1-rIcc=0 =>Icc=E/r=20/0,1=200 A
EXERCICE II:
1.
Quantité d’électricité au cours de la charge: QC=It=2X20=40 Ah
Quantité d’électricité au cours de la décharge: QD=8/10x40=32 Ah
La capacite est QD= 32 Ah
2. WC=ECQC=2,2x40=88 Wh
3. WD=EDQD=1,9x32=60,8 Wh
4.ID=32/10=3,2 A
.5.rW=60,8/88=0,69.
EXERCICE III:
1.
![]()
2.
Générateur: U=E-rI =>I=(E-U)/r=(46-41,5)/1,5=3 A
Batterie: U=E’ +r.I2 =>I2=(-E’+U)/r’=(-40+41,5)/1=1,5 A
Resistor: I1=I-I2=3-1,5=1,5 A
R1=U/I1=41,5/1,5=27,67Ω
EXERCICE IV:
1.
QD=IDt =>ID= QD/t=40/1=40 A
W=UIDt=11,8x40x1=472Wh
2. On utilise la batterie pour démarrer une automobile pendant 1,5 s. La batterie est alors traversée par un courant d’intensité 0,2 kA et la tension à ses bornes est de 10,2V.
(a) W=UIt=10,2x0,2103x1,5=3,06 KJ ou 0,85 Wh
(b) P=UI=10,2x0,2.103=2,04 KW
EXERCICE V:
1.On a au pôle négatif (production d’électrons) Pb = Pb2++ 2é.
Au pôle positif (consommation d’électrons) PbO2+ 4 H++ 2é = Pb2++ 2 H2O
2.En conditions standards on a E = E+- E-= E0PbO2/Pb2+- E0Pb2+/Pb= 1.58V
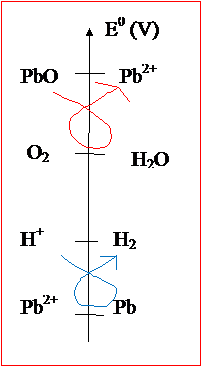
3.On peut représenter les couples sur une échelle:
On remarque que l’électrode recouverte de PbO2peut réagir avec l’eau (gamma rouge), et que celle en plomb peut réagir avec les ions H+de l’acide sulfurique (gamma bleu).
1. On a Q = 133 Ah = 133x3600 = 4.79 105C
![]()
![]()
Donc mPbO2= n0.MPbO2= 595 g