FORCE D’UN ACIDE ET D’UNE BASE
Acide:
Selon la théorie de Brönsted, un acide est tout corps susceptible de céder un proton H+ au cours d’une réaction chimique.
Exemple: L’acide chlorhydrique HCl
HCl → H+ + Cl-
Au cours de cette réaction, la molécule d’eau arrache un proton H+ a la molécule de chlorure d’hydrogène pour former l’ion hydronium H3O+. Ainsi, la molécule de HCl a cédé son proton à l’eau, HCl est un acide au sens de Brönsted.
L’équation bilan de la mise en solution du HCl est:
HCl + H2O → H3O+ + Cl-
Les solutions acides sont des solutions aqueuses ioniques qui contiennent des ions hydrogène H3O+ et des ions négatifs qui les accompagnent pour que la solution soit globalement neutre électriquement.
Autres acides: acide sulfurique H2SO4
acide nitrique:HNO3
Base:
Selon la théorie de Brönsted, une base est tout corps susceptible de fixer des protons H+ au cours d’une réaction chimique.
Exemple: L’hydroxyde de sodium NaOH
L’équation de mise en solution de NaOH est:
NaOH → Na+ + HO-
Les ions HO- réagissent sur les protons H+ pour former de l’eau selon l’équation:
HO- + H+ →H2O
Les ions HO- sont susceptibles de fixer des protons: NaOH est une base au sens de Brönsted.
Les propriétés de la solution aqueuse obtenue sont essentiellement celles des ions HO-. Les ions Na+ étant très peu réactifs.
Les solutions basiques sont des solutions aqueuses ioniques qui contiennent des ions hydroxyde HO- et des ions positifs qui les accompagnent pour que la solution soit globalement neutre électriquement
Autres bases: Ammoniac : NH3
Hydroxyde de potassium ou Potasse: KOH
Amphotère:
C’est une substance qui peut se comporter selon les conditions comme un acide de Brönsted et comme une base de Brönsted.
Exemple:
Une molécule d’eau s’ionise en libérant un proton selon l’équation:
H2O → HO- + H+
Le proton libéré est solvaté (hydraté) par une autre molécule d’eau selon l’équation:
H2O + H+→H3O+
Au cours de la première étape, l’eau cède un proton, elle se comporte comme un acide au sens de Brönsted. Au cours de la seconde étape, l’eau fixe un proton, elle se comporte comme une base au sens de Bronsted. L’eau peut se comporter, tantôt comme un acide, tantôt comme une base: c’est une substance amphotère.
Remarque:
On précise à chaque fois «au sens de Brönsted «parce qu’il existe une autre définition hors-programme des acides et bases au sens d’Arrhenius.
Acide fort
On appelle acide fort tout acide dont la réaction avec l’eau est totale.
Exemples: HCl, H2SO4 … sont des acides forts.
Réaction entre le chlorure hydrogène et l’eau
HCl + H2O→H3O+ + Cl-
Cette équation montre qu’en solution aqueuse, toutes les molécules HCl sont totalement ionisées.
La solution de HCl est représentée (H+ + Cl-)
NB: Le proton H+ s’associe à une molécule d’eau pour donner l’ion hydronium H3O+
La solution de HCl devient (H3O+ + Cl-)
Soit Ca, la concentration en ions H3O+,
c.-à-d. Ca = [H3O+]
pH=-log[H3O+] => pH=-logCa
Remarques:
-Cette formule ne s’applique pas à des solutions très diluées (Ca<10-6 mol.l-1), ni à des solutions très concentrées (Ca>5.10-2 mol.l-1)
-Elle n’est pas valable pour les polyacides.
Exemples: H2SO4
nH3O+=2nH2SO4 => pH=-log2Ca
Base forte
On appelle base forte toute base dont la réaction avec l’eau est totale.
En solution aqueuse toutes les molécules d’une base forte sont totalement ionisées.
Exemples: NaOH, KOH…sont des bases fortes.
L’ionisation dans l’eau d’une solution d’hydroxyde de sodium est une réaction totale d’équation:
NaOH → Na+ +HO-
La solution d’hydroxyde de sodium est représentée (Na+ + HO-)
Soit Cb, la concentration en ions OH-, c.-à-d.
Cb =[OH-]
A 25°C, [OH-]=10-14/[H3O+] =>[H3O+] =10-14/[OH-]=10-14/Cb =>
pH=-log[H3O+] => pH=-log10-14/cb => pH=14 + logCb
Remarques:
-Cette formule ne s’applique pas à des solutions très diluées (Cb<10-6 mol.l-1), ni à des solutions très concentrées (Cb>5.10-2 mol.l-1)
-Elle n’est pas valable pour les polybases.
Exemples: Ca(OH)2
NHO-=2n Ca(OH)2 , ![]() => pH=14+log2Cb
=> pH=14+log2Cb
Acide faible
Plus généralement, on appelle acide faible tout acide dont la réaction avec l’eau est partielle.
Un acide AH est faible si en solution aqueuse il est partiellement dissocié en ions H+ et en une base conjuguée A- .
AH + H2O ⇆ A- + H3O+
Example: acide éthanoïque (CH3COOH)
CH3COOH + H2O⇆CH3COO- + H3O
Base faible
Plus généralement, on appelle base faible toute base dont la réaction avec l’eau est partielle.
Une base A- est faible si en solution aqueuse elle s’associe partiellement à des ions H+ en produisant un acide conjugué AH.
A- + H2O ⇆ AH + HO-
Exemple: ion ethanoate (CH3COO-)
CH3COO- + H2O ⇆ CH3COOH +HO-
Degré d’ionisation
Le degré d’ionisation d’un acide ou d’une base est le nombre de moles dissociées par rapport au nombre de môles initiales.
α=ndissocie/ninitial
Cas d’un acide
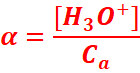
[H3O+] : concentration des ions H3O+ dans la
solution en fin de réaction
Ca : concentration initiale de l’acide avant sa réaction avec l’eau
Cas d’une base
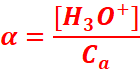
[HO-] : concentration
des ions HO- dans la solution en fin de réaction
Ca : concentration initiale de l’acide avant sa réaction avec l’eau
Remarque: Le degré d’ionisation augmente avec la dilution
EXERCICES
EXERCICE I:
On dispose des solutions acides et bases suivantes:
-A: acide chlorhydrique :C1=1,0.10-2 mol/l ; pH1=2,0
-B: acide éthanoïque :C2=5,0.10-2 mol/l ; pH2=3,1
-C: hydroxyde de sodium :C3=1,0.10-2 mol/l ; pH3=12,0
-D: ammoniac :C4=1,0.10-2 ; pH4=11,1
Donner, en justifiant, la force de chaque acide et de chaque base.
EXERCICE II:
On met en solution1 l de chlorure d’hydrogène pour obtenir 1 l d’une solution S0 d’acide chlorhydrique.
1.Determiner la concentration molaire de la solution S0 sachant que dans les conditions de l’expérience, le volume molaire est Vm=25 l/mol.
2.Determiner le pH de la solution S0.
3-Existe-t-il des molécules de HCl dans S0? Conclure
EXERCICE III:
Une solution commerciale d’hydroxyde de sodium a une densité d=1,38 et titre 35% d’hydroxyde de sodium en masse c.-à-d. que 1 kg de la solution contient 0,35 kg d‘hydroxyde de sodium.
1.Quelle est la concentration de cette solution commerciale?
2.Quel volume V1 de cette solution faut-il diluer dans l’eau pour obtenir 1 l de solution S1 de pH=12,5?
3.On verse 5 ml de la solution commerciale dans 1 l d’eau. Quel est le pH de la solution S2 obtenue?
4. Existe-t-il des molécules de NaOH dans S2? Conclure.
EXERCICE IV:
On dissout de l’acide éthanoïque CH3COOH dans l’eau. On obtient une solution de concentration Ca=10-2 mol/l, son pH est 3,4.
1.Donner l’équation d’ionisation de l’acide éthanoïque dans l’eau.
2.Quelles sont les espèces chimiques en solution?
3.Calculer les concentrations des espèces en solution
4.Calculer le pourcentage de dissociation de l’acide éthanoïque.
Déduire que c’est un acide faible.
EXERCICE V:
On dissout dans l’eau pure 1,125 g l’isomère CH3-CH2-NH2 de l’amine C2H7N ; le volume de la solution obtenue est 250 cm3. Le pH de la solution est 11,9.
1.Determiner la concentration molaire de la solution.
2.Ecrire l’équation de la réaction accompagnant la mise en solution de cette amine dans l’eau
3.Recenser les différentes espèces chimiques présentes dans la solution et déterminer leurs concentrations molaires.
4. Calculer le pourcentage de dissociation de l’amine. Conclure
On donne:C=12,0 g.mol-1; H=1,0g.mol-1; N=12 g.mol-1.
Avez-vous un exercice à proposer au Forum?Cliquez-ici
CORRIGES
Merci de votre
visite
Laissez un commentaire