NOTION DE QUANTITE DE CHALEUR.
Notion d’énergie
1. Définition
L’énergie est une grandeur physique qui représente la capacité d’un
corps ou d’un système à:
Déformer ou déplacer un corps.
- Élever
la température ou changer l’état physique d’un corps.
L’unité
de l’énergie dans le SI est le joule (j), il existe d’autres unités tel que le
wattheure (Wh) et 1Wh = 3600j.
Les
différentes formes d’énergie
L’énergie existe sous plusieurs
formes qui peuvent se transformer d’une à l’autre, les principales formes sont
: L’énergie électrique, mécanique (énergie potentielle de pesanteur, énergie
élastique, énergie cinétique), chimique, nucléaire, calorifique…
L’énergie calorifique se manifeste
sous forme de chaleur.
Notion de chaleur
2. Effets des échanges de chaleur.
Le transfert de chaleur
peut avoir pour effet:
- De
faire varier la température d’un corps ou système.
- De
provoquer un changement d’état physique.
- De
favoriser une réaction chimique.
Modes
de transfert de chaleur.
Les échanges de chaleurs peuvent se
faire soit par :
5.
La conduction: C’et la propagation de la
chaleur d’un point à un autre, (bâton en fer chauffé, la chaleur se propage
tout au long de celui-ci),
6.
La
convection: C’est le mouvement pris par un fluide dû aux différentes
températures ente les différentes parties du fluide (une eau chauffée, la
partie inférieure chauffée monte donnant place à celle supérieure),
7.
Le
rayonnement (une eau dans un verre et placé au soleil s’échauffe grâce au
rayonnement du soleil).
Mesure
des quantités de chaleur
Pour mesurer les quantités de
chaleur, généralement on utilise des appareils appelés calorimètres.
Ceux-ci sont des récipients fermés dont les parois sont constituées d’isolent
thermique. Ces parois ne permettent pas d’échanges de chaleur avec
l’extérieur: Les calorimètres sont donc considérés comme des enceintes
adiabatiques (les échanges de chaleur entre l’intérieur et l’extérieur sont
presque nuls).
Les calorimètres généralement utilisés
en laboratoire sont le calorimètre de Berthelot et le calorimètre de Dewar.
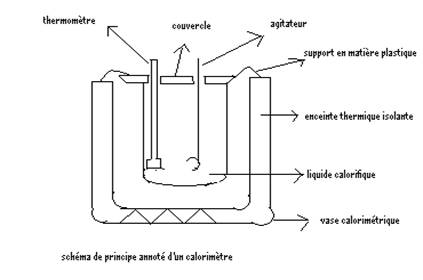
Principe des échanges de chaleur.
Lorsque plusieurs corps
sont dans une enceinte adiabatique, la somme algébrique des quantités de
chaleur échangées pour atteindre l’équilibre thermique est nulle:
∑Q = 0
3. Expression de la quantité de chaleur échangée par un corps ne
subissant pas de changement d’état.
L’expérience
montre qu’au cours de l’échauffement d’un corps, la quantité de chaleur Q reçue
par celui-ci est proportionnelle à sa masse et à la variation de sa
température. Ainsi, m représentant la masse de ce corps, et Δθ
la variation de température subit par le corps, nous aurons
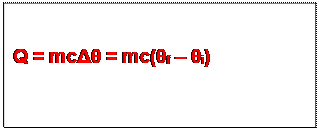
.
C est une constante qui dépend de la nature
du corps et est appelée chaleur massique de la substance constituant le
corps.
Exemple: CH2O=4190j/kg/K
![]() représente
la variation de température en kelvin(K)
représente
la variation de température en kelvin(K)
M est la masse du corps en kilogramme
(kg)
Q est la quantité de chaleur en
joules(J)
Relation entre
le degré Celsius et le degré kelvin
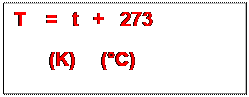
Remarques:
- Il existe
une autre unité pour la quantité de chaleur: La calorie (cal) et 1cal = 4,18j.
Dans
l’expression Q = mC(θf
– θi),
le produit mC généralement noté K est appelé capacité thermique ou capacité
calorifique du corps considéré d’où
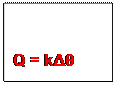
Capacité
thermique d’un calorimètre.
Généralement, le
calorimètre participe aux échanges thermiques. Il faut donc prendre en compte
la valeur de sa capacité thermique c ou k.
Expression de la
quantité de chaleur échangée par un corps qui subit un changement d’état.
La matière se présente
sous trois états physiques à savoir, l’état solide, liquide et gazeux. Très
souvent, pour passer d’un état à un autre, la matière peut:
- Soit
céder de la chaleur au milieu extérieur,
- Soit
en recevoir.
On
appelle chaleur latente de fusion d’un corps pur généralement noté Lf,
la quantité de chaleur à fournir à l’unité de masse de ce corps pris à sa
température de fusion pour l’emmener entièrement à l’état liquide. Cette
transformation s’effectue à température constante. Dans le SI, la
chaleur latente s’exprime en j/kg.
Dans le cas où l’on veut faire fondre une masse m d’un corps pris à sa
température de fusion, la quantité de chaleur nécessaire pour la fusion totale
de ce corps est donnée par la relation
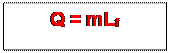 ,
,
Q
en joules(J)
m en kilogramme (kg).
Lf en joules par kilogramme(Jkg-1)
On
appelle chaleur latente de vaporisation
d’un corps pur notée Lv,
la quantité de chaleur qu’il faut
fournir à l’unité de masse de ce corps pur
pris à la température de vaporisation pour l’emmener entièrement à l’état
vapeur. Pendant ce changement la température reste constante. La chaleur
latente de vaporisation s’exprime en j/kg. Ainsi, pour vaporiser entièrement un
liquide de masse m pris à sa
température de vaporisation, la quantité de chaleur nécessaire donnée par la
relation
![]()
Q en joules(J)
men kilogramme (kg).
Lven
joules parkilogramme(Jkg-1)
EXERCICES
EXERCICE
I:
Calculer
la quantité de chaleur nécessaire pour porter une massed’eau
de 300g, initialement à 25°C à une température finale de 35°C.
On
donne la chaleur massique de l’eau: 4190 J.kg-1.K-1.
EXERCICE II:
On
mélange dans une enceinte adiabatique 5Ld’eau à
EXERCICE III:
Un
calorimètre contient une masse d’eau 200g à latempérature
18°C. On y ajoute une certaine quantité d’eau tiède de masse 100get de
température 25°C. A l’équilibre thermique, la température du mélange est20,3°C.
1-Quelle
est l’expression de la quantité de chaleur reçuepar
le système qui s’échauffe?
2-Quelle
est l’expression de la quantité de chaleur perduepar
le système qui se refroidit?
3-En
déduire la capacité calorifique du calorimètre.
EXERCICE IV:
1.
Déterminer la quantité de chaleur nécessairepour
faire fondre une massede 30g de
glace pris à 0°C.
On donneLf=
335j/kg.
2.
On désire chauffer une masse d’eau de 300g,initialement
à 25°C, jusqu’à la vaporisation. L’eau passe de l’état solide àl’état vapeur à 100°C sous la pression atmosphérique.
Calculer la quantité dechaleur reçue par cette masse
d’eau sachant que la chaleur latente devaporisation
de l’eau est de 2,25.106J.kg-1.
3.Quelle
quantité de chaleur faut-il fournir àun morceau de
plomb de masse m=200g, pris à latempérature θ1=25°C,
pour leporter à latempérature θ2=375°C.
On
donne:
-température
de fusion du plomb:θf=327°C;
-chaleur
latente de fusion du plomb:Lf=26,3.![]() J.kg-1.
J.kg-1.
-chaleur
massique du plomb à l’étatsolide :cs=129J.kg-1.
°C-1.
--chaleur massique duplomb
à l’état liquide :cL=142J.kg-1.°C-1.
EXERCICE V:
Situationproblème
L'étain est un corps solide à températureambiante. Il est utilisé pour la soudure des
composants électroniques.
Jean technicien de réparation des appareils électroniques, projette d'utiliserle dispositif ci-contre constitué de deux
thermoplongeurs pour faire fondre 100g de morceaux d'étain pris à 20'C en moins
de 5,0 s afin de respecter le timingde dépannage
imposé par les clients. Jean est préoccupé et se demande si ledispositif
sera à mesure de le satisfaire.
Par ailleurs compte tenu des contraintes financières, l'utilisation de cedispositif n'est possible que si le coût en énergie
électrique est négligeable( c'est-à- dire
inférieur à 1 Fcfasymbolique)en
10 s d'utilisation.
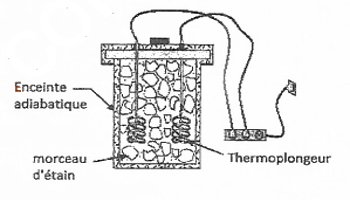
Document1 :
Caractéristique du système constitué par les deux thermoplongeurs.
Rendement estη=0,80
Puissance calorifique ( utile) Pc= 2,0kw
Document 2 : Coût énergétique
1kW.h = 3,6 405i
1kW.h coûte 75 Fcfa
Document 3 : Propriétés physiques de l'étain
Malléable et résiste à la corrosion.
Température de fusion :Tf= 232°C
Chaleur massique : C = 228 J/kg.K
Chaleur latente de fusion :Lf=
6000J/k
En exploitant les informations ci-dessus et en utilisant une démarchescientifique,
1 -Examine la préoccupation de Jean sur la capacité du dispositif à lesatisfaire.
2- Examine sur le pian financier s'il est possible d'utiliser cedispositif.
EXERCICEVI:
Situation problème :Vérification de la pureté du fer
Pour la construction d'un immeuble, un entrepreneur souhaite acheter du fer àBéton. Pour s'assurer de la pureté de celui-ci, il a
contacté le laboratoire dephysique d'un collège avec
un échantillon d'un kilogramme dudit fer. Celaboratoire,
dispose d'un calorimètre jamais utilisé dont la valeur en eaumarquée
estμ=18,2g, on y trouve aussi des dispositifs pourchauffer ou refroidir des corps. L'enseignant
responsable du laboratoire aréalisé les deux expériences
suivantes :
Expérience 1 :
Dans ce calorimètre contenant initialement 200 g d'eau à la température
de25,3°C, on verse 300 g d’eau à la température de 17,7 °C. On observe que latempérature du mélange se stabilise à 20,9°C.
Expérience 2 :
Dans le même calorimètre contenant 500 g d’eau à 20,9 °C, on plonge le bloc defer à la température de 48°C. La température se stabilise
à 14,2 °C.
Chaleur massique de l'eauce=419o J.kg/C, chaleur massique du ferpurcFe=470 J/kg.K
En exploitant les informations ci-dessus,
1 Prenez position sur la valeur en eau u qui est marquée.
2 À l'aide d'un raisonnement scientifique, prononcez-vous sur l'état de puretédu morceau de fer afin de permettre à l’entrepris de
se décider sur lacommande.
Avez-vous un exercice à proposer
au Forum?Cliquez-ici
Merci de votre visite
Laissez un commentaire