CORRIGES
EXERCICE I:
1.a
H3O+ ⇆ H2O + H+ =>couple H3O+/H2O
HO - +H+⇆H2O =>couple H2O/HO-
b.
L’ion H3O+ qui peut céder un proton H+ est un acide. Sa base conjuguée est la molécule d’eau.
L’ion HO- qui peut capter un proton H+ est une base, son acide conjugué est la molécule d’eau.
La molécule d’eau qui se comporte tantôt comme un acide et tantôt comme une base est un amphotère ou ampholyte.
2-a- couple HCl/Cl-
b-Le chlorure d’hydrogène est complètement ionisée. On ne retrouve plus les molécules de HCl dans la solution.
//la base conjuguée d’un acide fort est une espèce chimique indifférente dans l’eau.
EXERCICE II:
CH3COOH + H2O ⇆ CH3COO- + H3O+
1.Valeur
de l’expression 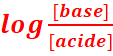
[H3O+]=10-pH=10-3,4
[CH3COO-]≈[H3O+]=10-pH=10-3,4
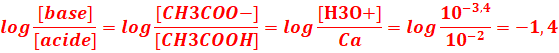
2.En déduire la valeur du pKA du couple CH3COOH/CH3COO-
pH=pKA + log [Base]/[Acide] =>pKA=pH- log [Base]/[Acide]=3,4+1,4 = 4,8
3.HCOOH→HCOO- + H3O+
[H3O+]=10-pH=10-2,9
pKA=pH- log [Base]/[Acide]=2,9-log10-2,9/10-2=2,9+0,9=3,8
A la même concentration, l’acide méthanoïque(pKA=3,8) est plus fort que l’acide éthanoïque(pKA=4,8).
EXERCICE III:
1.Equation d’ionisation de NH4Cl dans l’eau.
NH4Cl → NH4+ + Cl-
2.Calcul de la concentration initiale en ion ammonium.
[NH4+]=n/V=m/MV=0.32/(14+4+35,5)x0,1=0.06 mol.l-1
Montrons que l’ion ammonium est un acide faible.
[H3O+] =10-pH=10-5,2=6,3.10-6 mol.l-1.
[H3O+]<<[NH4+]=>[NH4+] est un acide faible
3.Ecrire l’équation bilan de la réaction entre l’ion ammonium et l’eau.
NH4+ + H2O → NH3 + H3O+
4.Le couple NH4+/NH3 a pour pKA=9,2.
4.1. Constante d’équilibre de cette réaction.

pKA=9,2.=> KA=10-9,2=6,3.10-10
4.2. Majoritaires : NH₄⁺, H₂O ; Minoritaires : NH₃, H₃O
//Cl- est un ion spectateur
EXERCICE IV:
1. Identifier le couple acide-base mis en jeu
La réaction :
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻
→ Le couple acide/base est : NH₄⁺ / NH₃
- NH₃ : base (capte un H⁺)
- NH₄⁺ : acide (donne un H⁺)
2. Calculer la constante de basicité Kb
On donne :
- Cb = 1,0 × 10⁻² mol/L
- pH = 10,6 → pOH = 14 - 10,6 = 3,4
- Donc : [OH⁻] = 10⁻³.⁴ ≈ 3,98 × 10⁻⁴ mol/L
À l’équilibre :
- [NH₄⁺] = [OH⁻] = x ≈ 3,98 × 10⁻⁴ mol/L
- [NH₃] ≈ Cb - x ≈ 1,0 × 10⁻² mol/L (x petit donc négligeable)
Kb = [NH₄⁺][OH⁻] / [NH₃]
Kb ≈ (3,98 × 10⁻⁴)² / (1,0 × 10⁻²) ≈ 1,58 × 10⁻⁵
3. Déduire Ka et pKa
On utilise : Ka × Kb = Ke = 1,0 × 10⁻¹⁴
Donc :
- Ka = Ke / Kb = (1,0 × 10⁻¹⁴) / (1,58 × 10⁻⁵) ≈ 6,33 × 10⁻¹⁰
- pKa = –log(Ka) ≈ –log(6,33 × 10⁻¹⁰) ≈ 9,2
4. Comparaison avec NaOH
- Ammoniac (1,0 × 10⁻² mol/L) : pH = 10,6
- NaOH (1,0 × 10⁻² mol/L) : pH ≈ 12
→ NaOH est une base forte, totalement dissociée
→ NH₃ est une base faible, partiellement protonée
EXERCICE V :
1- Il est question de se rassurer du titre molaire des solutions reçues.
Étapes :
• Écrire l'équation-bilan de la réaction support du dosage ;
• Déterminer le volume de la solution basique versé à l'équivalence ;
• Déterminer la concentration Cade la solution d’acide dosée ;
• Comparer la concentration Caà C;
• Conclure.
Résolution :
Équation-bilan de
la réaction :
AH+OH−→A−+H2O
Volume de base versé à l'équivalence :VbE=2VbE12=10mL
Détermination deCa
A l'équivalence on a :
nAH=nHO−⇒CaVa=CbVbE
Ca=CbVbE/Va=0,1 mol/L
Comparaison : On constate que Ca=C.
Conclusion : Le titre molaire des solutions reçues est bel et bien exact.
2- Identification de l'acide carboxylique présent dans les flacons.
Étapes :
• Déterminer la concentration en ions hydroxyde [HO−];
• Écrire l’équation d’électroneutralité (E.B.N) ;
• Déterminer la concentration des ions A−;
• Déterminer le Ka;
• Déduire le pKa;
• Retrouver sur le tableau le nom de l’acide AH correspondant au pKa trouvé.
Résolution :
Ke=[H3O+].[HO−]⇒[HO−]=Ke[H3O+]=7,1×10−11
mol/L
EEN :[N+a]+[H3O+]=[HO−]+[A−]⇒[A−]=[N+a]+[H3O+]
Car[HO−]≪[H3O+]
[A−]=0,0231mol/L
Ka=[H3O+][A−][AH]
AN :Ka=6,03×10−5.
pKa=−log(6,03×10−6)=4,2
En observant le tableau, on constate que l'acide faible correspondant à ce pKa
est l’acide benzoïque.
L'acide présent dans les flacons est donc l'acide benzoïque.