CORRIGES
EXERCICE I:
1.
Acides selon Brönsted : CH3COOH (acide acétique), HNO3(acide nitrique).
En solution ils libèrent un proton H+ qui s’associe à l’eau pour former l’ion hydronium H3O+(oxonium).
Bases selon Brönsted : NH3(ammoniac); KOH (hydroxyde de potassium ou Potasse).
En solution, ils libèrent l’ion HO- qui fixe un proton H+ pour former l’eau.
Amphotère : H2O.
2.
a) HCl + H2O →H3O+ + Cl-
b) NaOH → Na+ + HO –
c) H2SO4 + 2H2O → 2H3O+ + SO42–
3. Lorsqu'un acide réagit avec l'eau, il y a toujours formation d'ion hydronium H3O+.
Lorsqu'une base réagit avec l'eau, il y a toujours formation d'ion hydroxyde HO-.
EXERCICE II:
1.
1.1- volume de chlorure d’hydrogène obtenu
H2 + Cl2 → 2HCl
1mol 1mol 2mol
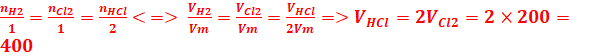 cm3.
cm3.
1.2-quantité en moles, de dihydrogène consommé
![]()
2.
2.1-concentration molaire de la solution obtenue
n=VHCl/Vm=0,120/24=5.10-3 mol
c=n/V=510-3 /0,25=2. 10-2mol.l-1.
2.2- concentration des ions hydronium ainsi que celle des ions chlorures
HCl + H2O → H3O+ + Cl-
1mol 1mol 1mol
[H3O+]=[Cl-]=[HCl]= 2.10-2mol.l-1.
EXERCICE III:
1.Hydroxyde de sodium: NaOH
M=23+16+1=40g.mol.l-1
C=n/V=m/MV=2,3/40x0,15=0,383 mol.l-1.
2.
2.1-masse de pastilles de soude
C1=1mol.l-1
C1=m/MV=>m=CVM=1x0,1x40=4 g
2.2- concentration molaire des ions hydroxydes dans la solution diluée
C1V1=C2V2 =>C2= C1V1/V2=1x10/1000=10-2 mol.l-1.
EXERCICE IV:
1. concentration en ions hydronium et hydroxyde
[H3O+]=10-pH =10-6,5=3,16.10-7 mol.l-1.
[HO+][HO-]=10-14 =>[HO-]=10-14/[H3O+]=10-14/3,16.10-7 = 3,16.10-8 mol.l-1.
2.La concentration des ions hydroxyde dans une solution aqueuse est égale à 10-4 mol.l-1.
2,1-Calcul de la concentration des ions hydronium et le pH de cette solution.
[H3O+][HO-]=10-14 =>[H3O+]=10-14/[HO-]=10-14/10-4=10-10 mol.l-1.
[H3O+]=10-pH=10-10 => pH=10.
2.2- couleur prise dans cette solution :
a- bleu
b-rose violace
c-jaune
2.3-
b- solution d’hydroxyde de sodium car pH>7
EXERCICE V:
1. concentration C de la solution
M=23+16+1=40g.mol.l-1
C=n/V=m/MV=2/40x0,25=0,2 mol.l-1
2. concentrations des ions hydroxyde et hydronium
[HO-]=C=0,2 mol.l-1
[H3O+] =10-14/[HO-]=10-14/0,2=5.10-14 mol.l-1
3. pH de la solution
pH=-log[H3O+]=-log5.10-14=13,3.
EXERCICE VI:
1. masse de chlorure d’hydrogène et volume d’ammoniac
CA=CB =0,1 mol.l-1 //solution decimolaire
VA=VB=250 ml
nA=CAVA=0,1x0,25=0,025 mol
nA=mA/MA => mA=nAxMA=0.025x36,5=0,91 g
nB=CBVB=0,1x0,25=0,025 mol
nB=VB/Vm => VB=nBVm =0,025x24=0,6 l.
2.équations bilans traduisant l’action de l’eau sur le chlorure d’hydrogène et l’ammoniac.
HCl + H2O →H3O+ + Cl-
NH3 + H2O ⇆ NH4+ + HO-
3.
Acide: Selon la théorie de Bronsted, un acide est tout corps susceptible de céder un proton H+ au cours d’une réaction chimique.
Base: Selon la théorie de Bronsted, une base est tout corps susceptible de fixer des protons H+ au cours d’une réaction chimique.
4.
Acide: HCl, H2O
Base: NH3, H2O // l’équation de la deuxième réaction traduit un équilibre. Dans ce cas NH4+ est acide au cours de la réaction inverse. C’est l’acide conjugué de la base NH3 (cours Tle)
5.Amphotère.L’eau est un ampholyte.
6.pH=-logCA=-log0,1=1 // la solution A est acide de pH=-logCa.
7. non, c’est une base faible. La dissociation n’est pas totale. //Pour trouver le pH, la notion de constante d’acidité pKA intervient (cours Tle)
8. le pH de la solution B est supérieur à celui de l’eau pure (pH>7).
EXERCICE VII:
1.
S1:pH=3,8
S2:[HO-]=10-3 mol.l-1=>[H3O+]=10-14/[HO-]=10-14/10-3=10-11 =>pH=11
S3:[H3O+]=[HO-] =>pH=7
S4:[H3O+]=5.10-3 mol.l-1=>pH=-log5.10-3=2,3
S5:pH=8
Classement:S2,S5,S3,S1,S4
2.pH=-log2c=-log2x5.10-4=-log10-3=3 //c’est un diacide.