CORRIGES
 EXERCICE
I:
EXERCICE
I:
1. Formule semi-développée de l’acide aspartique
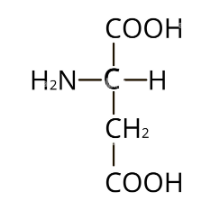
2. Groupes fonctionnels présents dans cette molécule
─ NH2 : groupe amine
─COOH : groupe carboxylique
3. Nom en nomenclature systématique de l’acide aspartique.
Acide 2-aminobutane-1,4-dioique
EXERCICE II:
1. Formules semi-développée possibles
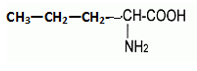 Acide 2-aminopentanoique
Acide 2-aminopentanoique
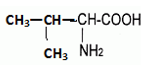 Acide 2-amino
3-methylbutanoique (valine)
Acide 2-amino
3-methylbutanoique (valine)
// Acide 2-amino-2-méthylbutanoïque
CH3
|
H3C–CH(NH2)–CH2–COOH
(NB : ce dernier n’est pas un acide α-aminé au sens strict car le groupe NH2 n’est pas sur le carbone α du COOH.)
2.
Acide 2-aminopentanoïque
(CH3–CH2–CH2–CH(NH2)–COOH)
→ Le carbone α (celui portant –NH2) est lié à :
- un groupe –NH2
- un groupe –COOH
- un groupe –CH2CH2CH3
- un hydrogène
⇒ Il est asymétrique
. Acide 2-amino-3-méthylbutanoïque
((CH3)2CH–CH(NH2)–COOH)
→ Le carbone α est lié à :
- un groupe –NH2
- un groupe –COOH
- un groupe isopropyle (–CH(CH3)2)
- un hydrogène
⇒ Il est asymétrique
⇒ Il est asymétrique
3.
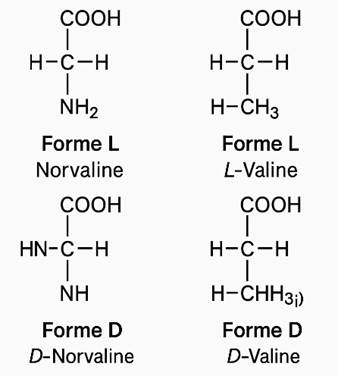
EXERCICE III:
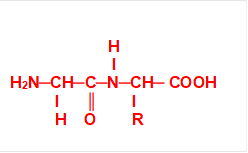
1. Formule générale d’un acide ɑ-aminé.
R─CH─COOH
I
NH2
 2. Nature du
radical de X.
2. Nature du
radical de X.
M=MR+ 7+28+48+48= MR+131 <=> 132= MR+131 =>MR=1
C’est l’atome d’hydrogène
3. Formule semi-développée et le nom de X.
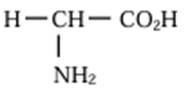
Sa molécule n’est pas chiralecar il n’y a pas de carbone asymétrique.
EXERCICE IV:
1. Formule brute de A.
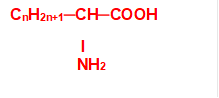 |
M=12n +2n+1 +24+4+14+32=14n+75 <= > 131=14n+75. => n =4
Formule brute:C6H13O2N
2. Formule semi-développée.
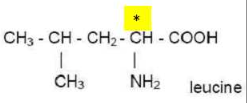 Acide 2-amino
4-methylpentanoique
Acide 2-amino
4-methylpentanoique
3. En solution aqueuse, le groupe acide carboxylique (-CO2H)
de A a tendance à céder un proton H+ (acide de Bronsted) alors
que
le
groupe amine (-NH2) de A a
tendance à capter un proton H+ (base de Bronsted).
A présente donc à la fois un caractère acide et un caractère basique:
C’est un amphotère.
EXERCICE V:
1.
1.1.Le nom systématique de la valine : Acide 2-amino-3-methylbutanoique
1.2.Le nom du type de liaison dans D La liaison peptidique
2. J’explique ce qu’il faut faire Il faut d’une part bloquer ou désactiver les groupes qui participent aux réactions non souhaitées et d’autre part activer l’un des groupes participant à la réaction voulue.
3. J’écris l’équation.
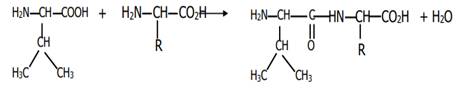
4. Je détermine le groupe alkyle R : La formule de R est 𝐶𝑛𝐻2𝑛+1 𝑀(𝑅 −) = 12𝑛 + (2𝑛 + 1) + 1 = 14𝑛 + 1 𝑀(𝑅 −) = 𝑀 − (7𝑀𝐶 + 13𝑀𝐻 + 7𝑀𝑁 + 3𝑀𝑂) = 188 − (7 × 12 + 13 × 1 + 2 × 14 + 3 × 16 𝑀(𝑅 −) = 15 14𝑛 + 1 = 15 𝑛 = 15−1 14 = 1 ⇒ 𝑅 − 𝑒𝑠𝑡 𝑙𝑒 𝑔𝑟𝑜𝑢𝑝𝑒 𝑚𝑒𝑡ℎ𝑦𝑙𝑒 (𝐶𝐻3−)
5. J’identifie B Formule semi-développée : Nom : Acide 2-aminopropanoique (Alanine).