CORRIGES
EXERCICE I
1. Formule brute générale: CnH2nO2.
%O=(2X16/M)x100 =>M=3200/%O=3200/(100-(58,8+9) =101,91g/mol
M=14n +32=101,91 <= >14n=69,91 => n=5
Formule brute: C5H10O2
2.Acide 2-methylpropanoique
.CH3-CH(CH3)-COOH
EXERCICE II:
1, CnH2n+1-COOH
2. CH3-OH: methanol
3.Équation de la réaction.CH3-OH+ CnH2n+1-COOH⇌ CnH2n+1-COOCH3+H2O
M=14n+60 = 88=> n=2
Formule réelle:C2H5-COOH(Acide propanoïque).
4. On note C le chlorure d’acyle dérivé de l’acide A
Formule semi-développée de C: C2H5-COCl
On fait agir l’acide avec du chlorure de thionyle (SOCl2)
C2H5-COOH + SOCl2→ C2H5-COCl +SO2+HCl
-réaction de C sur B Plus rapide, totale et exothermique.
EXERCICE III:
1-C2H5OH+
CH3-COOH ⇌![]() CH3-COO(C2H5)
+ H2O
CH3-COO(C2H5)
+ H2O
Compose B: Ethanoate d’ethyl
2-esterification
3- Macid=2x12+4+2x16=60 g/mol, Mest=102 g/mol

EXERCICE IV:
1.Formule de A: CxHyOz
M=29d=29x2,07=60,03g
![]()
![]()
![]()
=>C3H8O
2-
2.1. Equation bilan de la réaction:
C3H7OH+
C2H5-COOH⇌![]() C2H5-COO(C3H7)
+ H2O
C2H5-COO(C3H7)
+ H2O
Rôle de l’acide sulfurique: Catalyseur
Nom du composé organique obtenu:
Propanoate de propyl
2.2.![]() =>
=>![]()
![]()
![]()
EXERCICE V:
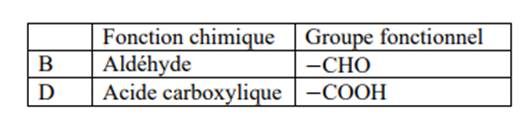
1.Fonction chimique et groupe fonctionnel de B et D
2.2.1. Équation –bilan de la réaction acido-basique :
![]()
2.2.A l'équivalence acido-basique CaVa = CbVBe, la valeur de Ca = 5.10-3mol.L-1
![]()
On pose alors 14n +32 = 74 d’où n = 3
La formule brute est : C3H6O2
2.3.Nom et formule semi-développée de D :
2.4.CH3CH2COOH : acide propanoïque
3.1.
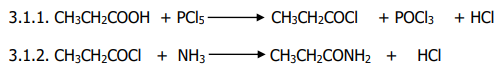
3.3. Nom : Propanamide, fonction chimique : Amide