CORRIGES:
EXERCICE I
1. Formule électronique du sodium: K2L8M1;
un seul électron de valence (périphérique).il a tendance à perdre cet électron
pour devenir l’ion Na+.
2. Formule électronique du chlore: K2L8M7;
il a tendance à gagner un électron pour saturer sa derrière couche (avoir
8 électrons sur la dernière couche conformément à la règle de l’octet).
Formule chimique de l’ion monoatomique issu du chlore: Cl-
3. Un atome est stable lorsque sa dernière couche est saturée à 2, 8…électrons.
Ainsi, Na+ veut se débarrasser de son unique électron externe pour avoir 8 électrons de valence. De même Cl- a besoin d’un électron pour saturer la sienne. Lorsqu’ils se trouvent ensemble, il y a mise en commun des deux électrons célibataires pour créer une liaison covalente: Na-Cl
EXERCICE II:
1. Structures électroniques de Mg: K2L8M2
Structures électroniques de Cl: K2L8M7
2. Charge des ions Mg: +2
Charge des ions Cl: -1
3. Ces ions possèdent sur leurs couches externes: 2 pour Mg et 7 pour Cl
EXERCICE III:
1. Formule électronique: K2L4 pour le carbone et K2L5 pour l’azote
Représentation de
Lewis: ![]() pour le carbone et
pour le carbone et ![]() pour l’azote
pour l’azote
Valences: 4 pour le carbone et 3 pour l’azote.
2. Formule développée du méthane
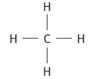
Formule développée de l’ammoniac.
H&;N&H
H
1)3.1.
a) Electronégatifs: I S°° I O°°
b) Electropositifs: °Zn° °Sr° °Ba°
3.2. S2- ; O2- Zn2+ Sr2+ Ba2+.
EXERCICE
IV :
1. 7 électrons
2. 3 électrons
3. Groupe 2 et Période 3
4. K2L8M5
EXERCICE V:
1. Le soufre a 6 électrons de valence. Les 4 premiers sont dessinés non appariées, puis on apparie les deux derniers. Le schéma de Lewis correct est donc le (b).
2. F, Cl et Br: 17e colonne =>7 électrons de valence.
![]()
Avez-vous un exercice à proposer ?Cliquez-ici
Merci de votre visite
Laissez un commentaire