CORRIGES
EXERCICE I:
1. formules semi-développées des hydrocarbures :
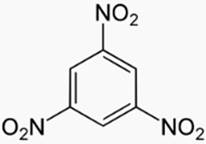
a) 1, 3, 5-trinitrobenzène
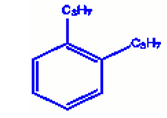
b) Orthodipropylbenzène
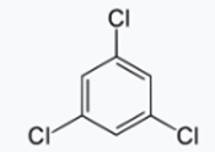
c) 1, 3, 5-trichlorobenzène
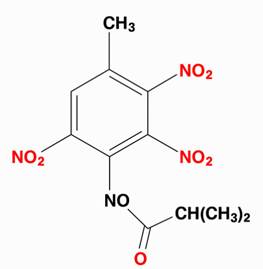
d) 2, 4, 6-trichlorotoluène
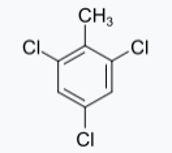
2.
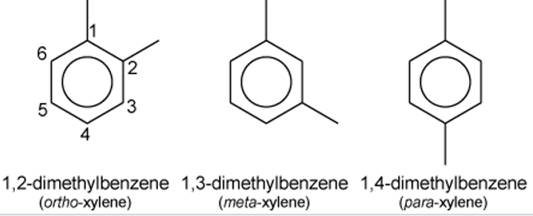
a) isomères aromatiques du diméthylbenzène.
Lexylène, oudiméthylbenzène, est un groupe d'hydrocarbures aromatiquesdérivésméthylésdubenzène. Il est représenté par troisisomèresstructuraux: 1,2-diméthylbenzène, 1,3-diméthylbenzène et 1,4-diméthylbenzène (appelés respectivement ortho-diméthylbenzène, méta-diméthylbenzène et para-diméthylbenzène).
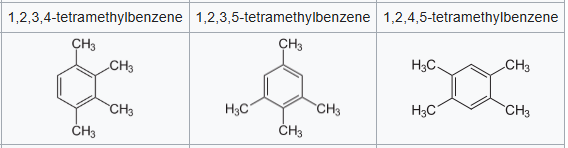
b) isomères de tétraméthylbenzène.
Ledurèneou 1,2,4,5-tétraméthylbenzène est unhydrocarbure aromatiquedérivé dubenzène. C'est un intermédiaire dans la synthèse de l'acide pyromellitique qui est utilisé pour la fabrication d'agents de durcissement, decolleset de matériaux de revêtement. Il est utilisé dans la fabrication de certaines matières premières pour les plastiques techniques (polyimides) et d'agent de réticulationpour lesrésinesglycéro
3. formules semi-développées des composés ayant pour formules brutes C8H10.
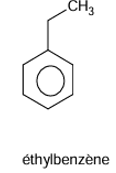
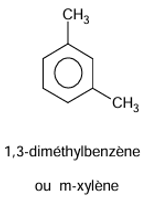
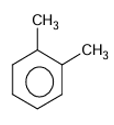
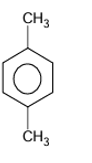

EXERCICE II:
1) formule brute du composé: CxHy
![]() =
=![]()
![]() =
=![]()
formule brute: C6H6
2)
a) Nommons le corps A et donnons sa formule développée.
b)
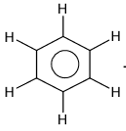
C’est le benzène
b) équation de la réaction.
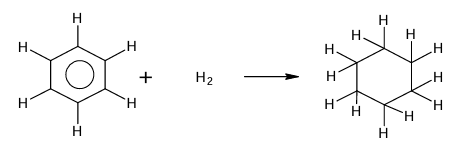
Nom de la réaction: hydrogénation
3) volume de dihydrogène mesuré dans les CNTP
n=m/M=19,5/78=0,25 mol
n=V/Vm =>V=nVm=0,25x22,4=5,6 l
EXERCICE III:
1) équation de la réaction qui se produit
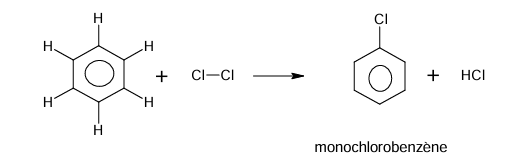
2) Nommons le produit obtenu: monochlorobenzène.
Chloration du benzène
3) masse du produit obtenu sachant que le benzène est en excès.
On donne : masse molaire Cl : 35.5 g/mol ; R = 8.31 constante des gaz parfaits
PV=nRT=>n=PV/RT=105X10.10-3/8,31x300=0,4 mol
M=nM=0,4x112,5=45 g
EXERCICE IV:
1.Calcul du volume de HCl
C6H6 + Cl2 →C6H5Cl + HCl
1 mol 1mol 1mol 1mol
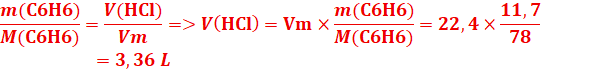
2.
a. Équation globale (simplifiée) :
C₆H₅CH₃ + 3 HNO₃ → C₆H₂(CH₃)(NO₂)₃ + 3 H₂O
(Toluène → TNT
b. Masses molaires
- Toluène (C₇H₈) : 92 g/mol
- TNT (C₇H₅N₃O₆) : 227 g/mol
Donc, 1 mole de toluène (92 g) donne 1 mole de TNT (227 g).
- 92 g de toluène → 227 g de TNT
- 23 000 g de toluène → x g de TNT
x = (227 × 23 000) / 92 ≈ 56 760 g = 56,76 kg
3. 354,5 g.mol-1;50,1%;37,5 g.
a. Calcul de la masse molaire (M) du DDT :
- C (carbone) : 14 × 12,01 = 168,14 g/mol
- H (hydrogène) : 9 × 1,008 = 9,072 g/mol
- Cl (chlore) : 5 × 35,45 = 177,25 g/mol
Masse molaire totale ≈ 168,14 + 9,072 + 177,25 = 354,46 g/mol
b. Pourcentage massique de chlore dans le DDT :
%Cl = (177,25 / 354,46) × 100 ≈ 50,0 %II:
c. 0,5 g de DDT par kg de masse corporelle est mortelle.
Homme de 75 kg :
- Masse mortelle = 0,5 g × 75 kg = 37,5 g
EXERCICE V:
1. Formules semi développées des composés susceptibles de se former.
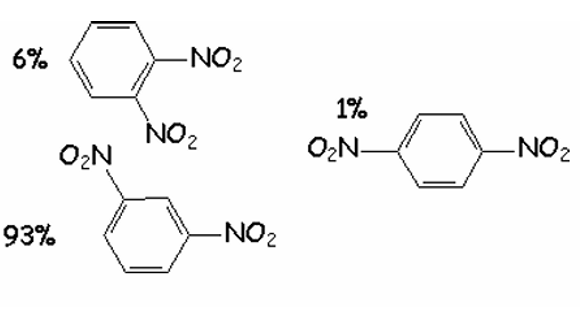
Calcul de la masse totale de dinitrobenzène obtenue à partir de 50 g de benzène, en supposant une nitration complète (ajout de deux groupes –NO₂) et un rendement de 100 %.
Données nécessaires
- Masse molaire du benzène (C₆H₆) = 78 g/mol
- Masse molaire du dinitrobenzène (C₆H₄(NO₂)₂) = 168 g/mol
- Masse de benzène utilisée = 50 g
- Pourcentages dans le mélange :
- ortho : 6 %
- méta : 93 %
- para : 1 %
· Calcul du nombre de moles de benzène
n = m / M = 50 / 78 ≈ 0,641 mol
Masse totale de dinitrobenzène produite
1 mol de benzène donne 1 mol de dinitrobenzène (réaction 1:1)
Donc :
0,641 mol de benzène → 0,641 mol de dinitrobenzène
m = n × M = 0,641 × 168 ≈ 107,9 g
→ On obtient environ 108 g de dinitrobenzène (toutes formes confondues).
· Répartition selon les isomères
- ortho : 6 % de 108 g = 6,48 g
- méta : 93 % de 108 g = 100,44 g
- para : 1 % de 108 g = 1,08 g
2.On chlorure 3,0 g de benzène (C₆H₆) en présence de AlCl₃.
Le rendement est de 80 %.
On cherche la quantité de monochlorobenzène (C₆H₅Cl) obtenue, en mole et en gramme.
Données :
- M(Benzène) = 78 g/mol
- M(Monochlorobenzène) = 112,5 g/mol
· Étapes de résolution :
Équation de la réaction :
C₆H₆ + Cl₂ → C₆H₅Cl + HCl
C’est une réaction 1:1 (1 mol de benzène donne 1 mol de C₆H₅Cl)
· Calcul du nombre de moles de benzène :
n(C₆H₆) = 3,0 g / 78 g/mol = 0,0385 mol
3. Rendement de 80 % ⇒ moles de C₆H₅Cl obtenues :
n(C₆H₅Cl) = 0,0385 × 0,80 = 0,0308 mol
· Masse de C₆H₅Cl obtenue :
m = n × M = 0,0308 mol × 112,5 g/mol = 3,47 g
Réponse finale :
- n(C₆H₅Cl) = 0,0308 mol
- m(C₆H₅Cl) = 3,47 g
3.
a. Équation de la réaction :
C₆H₅CH₃ + Cl₂ → C₆H₅CH₂Cl + HCl
C’est une substitution radicalaire : un atome d’hydrogène sur le groupement méthyle est remplacé par un atome de chlore.
b. Nombre de moles de toluène utilisées :
m = 5,0 g
M = 92 g/mol
n = m / M = 5,0 / 92 ≈ 0,054 mol
c. Rendement = 75 %
Si la réaction était totale, on obtiendrait :
n(théorique) = 0,054 mol de C₆H₅CH₂Cl (car rapport 1:1)
Mais avec un rendement de 75 % :
n(réelle) = 0,75 × 0,054 ≈ 0,0405 mol
Masse de chlorure de benzyle obtenue :
M = 126,5 g/mol
m = n × M = 0,0405 × 126,5 ≈ 5,12 g
EXERCICE VI:
1. Équation de la réaction (simplifiée) :
C₆H₆ + 2 Cl₂ → C₆H₄Cl₂ + 2 HCl
Un benzène donne un 1,4-dichlorobenzène (PDCB)
- Masse de PDCB produite : 100 g
- Masse molaire du PDCB = 147 g/mol
- Masse molaire du benzène = 78 g/mol
- Rendement : 60 % (soit 0,60)
Calcul de la quantité de PDCB voulue (en mol)
n(PDCB) = 100 / 147 ≈ 0,680 mol
Comme le rendement est de 60 %, la quantité de benzène théorique nécessaire est :
n(C₆H₆) = 0,680 / 0,60 ≈ 1,133 mol
Masse de benzène nécessaire :
m = n × M = 1,133 × 78 ≈ 88,4 g
2.
- Masse du composé analysé : 12,3 mg
- M (masse molaire) du composé : 112,5 g/mol
- CO₂ produit : 289 mg
- H₂O produite : 4,9 mg
- Masse de composé pour analyse du chlore : 8,7 mg
- Masse de AgCl obtenue : 11,1 mg
a) Détermination de la formule brute
Trouvons le nombre de moles de C, H, Cl
Carbone (C)
CO₂ contient 1 atome de C
M(CO₂) = 44 g/mol
→ moles de C = 289 mg / 44 g/mol = 6,57 mmol
Masse de C = 6,57 × 12 = 78,8 mg
Hydrogène (H)
H₂O contient 2 atomes de H
M(H₂O) = 18 g/mol
→ moles d’H = (4,9 / 18) × 2 = 0,544 mmol × 2 = 1,089 mmol
Masse d’H = 1,089 × 1 = 1,089 mg
Chlore (Cl) via AgCl
M(AgCl) = 143,5 g/mol
→ moles de AgCl =…
Convertissons les moles en ratios :
- C = 6,57 mmol
- H = 1,089 mmol
- Cl = 0,0774 mmol
Divisons par le plus petit :
- C = 6,57 / 0,0774 ≈ 85
- H = 1,089 / 0,0774 ≈ 14
- Cl = 0,0774 / 0,0774 = 1
→ Approximation : C₆H₅Cl (rapport de C:H:Cl ≈ 6:5:1)
Vérifions la masse molaire
C₆H₅Cl → (6×12) + (5×1) + (1×35,5) = 72 + 5 + 35,5 = 112,5 g/mol
Conclusion :
- Formule brute : C₆H₅Cl
- Formule développée : c’est le chlorobenzène (un noyau benzénique avec un Cl en substitution).
b) Quelle masse de dichlore (Cl₂) faut-il pour 8,7 mg de composé ?
Réaction :
C₆H₆ + Cl₂ → C₆H₅Cl + HCl
→ 1 mol de C₆H₆ nécessite 1 mol de Cl₂
Moles de C₆H₅Cl = 8,7 mg / 112,5 = 0,0773 mmol
Donc il faut 0,0773 mmol de Cl₂
Masse de Cl₂ = 0,0773 × 71 = 5,49 mg
Conclusion :
- Il faut environ 5,49 mg de Cl₂ pour obtenir 8,7 mg de chlorobenzène à partir du benzène
3. Pour résoudre cet exercice, on suit les étapes suivantes :
Données :
- Masse de naphtalène (C₁₀H₈) = 15 g
- Masse molaire du naphtalène = 128 g/mol
- Réaction : nitration du naphtalène → C₁₀H₇NO₂ (nitronaphtalène)
- Masse molaire de C₁₀H₇NO₂ = 173 g/mol
- Rendement = 90%
· Réaction chimique simplifiée :
C₁₀H₈ + HNO₃ → C₁₀H₇NO₂ + H₂O
→ 1 mol de naphtalène donne 1 mol de nitronaphtalène
Calcul des moles de naphtalène :
n = 15 g / 128 g/mol = 0,1172 mol
· Moles de nitronaphtalène obtenues (avec 90% de rendement) :
n(produit) = 0,1172 × 0,90 = 0,1055 mol
· Masse obtenue de nitronaphtalène :
m = 0,1055 mol × 173 g/mol = 18,26 g
Résultat final :
On peut obtenir environ 18,26 g de nitronaphtalène à partir de 15 g de naphtalène avec un rendement de 90
EXERCICE VII:
1. Le xylène a troisisomèresstructuraux: 1,2-diméthylbenzène, 1,3-diméthylbenzène et 1,4-diméthylbenzène (appelés respectivement ortho-diméthylbenzène, méta-diméthylbenzène et para-diméthylbenzène).
2. Le propène peut fixer une molécule de chlorure d’hydrogène.
a) formules développées des deux produits que l’on peut obtenir
CH3-CH=CH2 + HCl → CH3-CHCl-CH3 ou CH3 -CH2-CH2Cl
b) le plus symétrique des deux est:
CH3-CHCl-CH3 2-chloropropane
3.
a) Voici les isomères possibles issus de la réaction du méta-xylène (1,3-diméthylbenzène) avec le 2-chloropropane (CH₃–CHCl–CH₃) en présence d’un catalyseur (AlCl₃) :
Rappel :
Le méta-xylène a des groupes CH₃ en positions 1 et 3 sur le noyau benzénique.
L’isopropyle (–CH(CH₃)₂), obtenu par alkylation, peut s’ajouter sur les positions 2, 4, 5 ou 6, en tenant compte des effets directeurs des CH₃.
Isomères possibles (triméthylbenzènes ramifiés) :
1,3-diméthyl-2-isopropylbenzène
1,3-diméthyl-4-isopropylbenzène
1,3-diméthyl-5-isopropylbenzène (produit principal, positions para et ortho activées)
1,3-diméthyl-6-isopropylbenzène
Ces isomères sont tous des isomères de position (même formule brute, groupements situés à des positions différentes sur le noyau aromatique)
Le produit principal est un triméthylbenzène substitué par un groupe isopropyle (–CH(CH₃)₂) sur le noyau aromatique.
CH3
|
/¯¯¯¯¯¯\
CH3–| |–CH(CH3)2
\___ _/
Explication :
- Le méta-xylène a deux groupes –CH₃ en position 1 et 3.
- L'isopropyle (issu du 2-chloropropane) vient s’ajouter en position 5 (par rapport au groupe 1), dirigé par les deux CH₃.
- Le composé obtenu est 1,3-diméthyl-5-isopropylbenzène
b)
Compte tenu de l’encombrement stérique du groupe isopropyle (–CH(CH₃)₂), l’isomère le plus abondant sera celui où ce groupe se fixe le plus loin possible des deux groupes méthyles (–CH₃) déjà présents sur le méta-xylène.
Raisonnement :
Le méta-xylène a ses deux groupes CH₃ en positions 1 et 3.
Le groupe isopropyle, issu de l’alkylation, s'ajoute préférentiellement en position :
C’est la position para par rapport au CH₃ en position 1, et méta par rapport au CH₃ en position 3.
➤ C’est la moins encombrée.
Conclusion :
L’isomère 1,3-diméthyl-5-isopropylbenzène sera le plus abondant, car il minimise les répulsions stériques entre les substituants.
Formule brute : C₁₁H₁₆
4. formule brute: CxHyNzOt
Données :
- C : 46,6 %
- H : 4,6 %
- N : 14,8 %
- O : 33,9 %
![]() =
=![]()
![]() =
=![]()
![]() =
=![]()
![]() =
=![]()
- C ≈ 11
- H ≈ 13
- N = 3
- O ≈ 6
Donc formule brute probable : C₁₁H₁₃N₃O₆
Masse molaire :
- C₁₁ : 11 × 12 = 132
- H₁₃ : 13 × 1 = 13
- N₃ : 3 × 14 = 42
- O₆ : 6 × 16 = 96
Masse molaire ≈ 132 + 13 + 42 + 96 = 283 g/mol
Formule développée possible :
Le composé de départ est 1,3-diméthyl-5-isopropylbenzène (C₁₁H₁₆). Une nitration remplace un atome H du noyau aromatique par un groupe –NO₂.
Mais ici, on a 3 atomes d'azote et 6 d'oxygène, soit 3 groupes –NO₂
Donc : le composé obtenu est probablement un dérivé trinitré du diméthylisopropylbenzène.
Nom :
1,3-diméthyl-5-isopropyl-2,4,6-trinitrobenzène
C'est un dérivé de type trinitrotoluène modifié