CORRIGES
EXERCICE I:
1.Le 2,2-diméthylpropane
2. Le 2-méthylbutane
3. Le 2,4-dimethylhexane
4. Le 2,2,4-trimethylpentane
5. Le 2,3-dimethylpentane
EXERCICE II:
1.
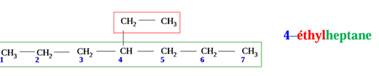
2.
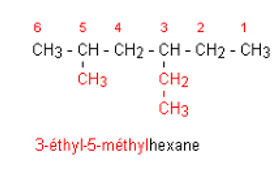
3.
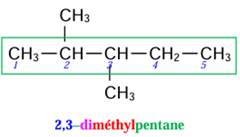
4.
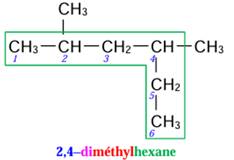
5.
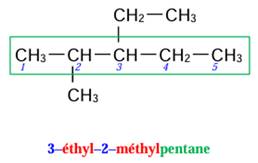
EXERCICE III:
1.
a-équation-bilan de la réaction.
C3H8+2O2→3CO2+ 4H2O
b- volume de CO2 obtenu
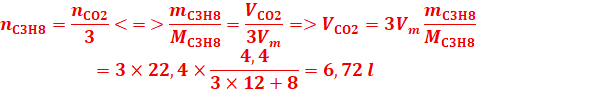
2.
a- volume de méthane
CH4+ 2Cl2→ C + 4HCl
![]()
b- volume de dichlore
![]()
3. Données :
- Volume initial du mélange C₂H₆+ C₃H₈= 40 cm³
- Dioxygène introduit = 200 cm³
- Gaz résiduels après combustion = 127,5 cm³
- Absorbés par potasse (absorbe CO₂) : 105 cm³
- Le reste (127,5 - 105 = 22,5 cm³) est absorbé par le phosphore (absorbe O₂non consommé)
Réactions de combustion :
Éthane :
C₂H₆+ (7/2) O₂→ 2 CO₂+ 3 H₂O
Propane :
C₃H₈+ 5 O₂→ 3 CO₂+ 4 H₂O
On note :
- x = volume de C₂H₆dans le mélange
- y = volume de C₃H₈
Avec :
x+ y = 40…(1)
Volume de CO₂formé = 105 cm³ (absorbé par potasse)
CO₂formé = 2x (par C₂H₆) + 3y (par C₃H₈)
Donc :
2x + 3y = 105…(2)
Résolvons les deux équations :
(1) x + y = 40
→ y = 40 - x
Remplaçons dans (2) :
2x + 3(40 - x) = 105
2x + 120 - 3x = 105
-x + 120 = 105
x= 15
y= 25
Conclusion :
Le mélange initial était composé de :
- 15 cm³ d’éthane (C₂H₆)
- 25 cm³ de propane (C₃H₈)
EXERCICE IV:
1.Masse volumique (kg / m3) du liquide : 10 L = 0,01 m3(1000 L= 1m3) masse (kg) / volume (m3) = 7 /0,01 = 700 kg /m3
2.masse volumique (kg / m3) du gaz : cette masse volumique dépend de la température et de la pression dans les conditions normales de température et de pression le volume molaire d'un gaz est 22,4 L = 0,0224 m3.
Masse molaire du propane C3H8 :12 .3+8 = 44 g/mol = 0,044 kg / mol0,044 / 0,0224 = 1,96kg/m3
.3. Densité d'un gaz par rapport à l'air d = masse molaire (g/mol) / 29 = 44/29 = 1,51 le propane est plus dense que l'air volume de gaz :
4.Quantité de matière (mol)= masse (g) / masse molaire (g/mol) = 7000 /44 = 159 mol
Volume (L) = volume molaire (L/mol) x Qté de matière (mol) = 22,4*159 = 3562 L.
5.combustion : C3H8+ 5O2→ 3 CO2+ 4H2O
Qté de matière de dioxygène : 5. 159 = 795 mol volume O2 : 22,4 .795 = 17 800 L = 17,8 m3.
L’air contient en volume environ 20% de dioxygène.17,8. 5 = 89 m3d'air.
6. A partir de 1L de propane gaz : 1 /22,4 = 0,0446 mol = 44,6 mol propane donc 4. 0,0446 = 0,178 mol d'eau 6.
Masse molaire de l'eau : 18 g/mol masse d'eau :18 .0,178 =3,21 g.
EXERCICE V:
Masse molaire : propane : 3x12+8=44 g/mol ;
CO2:12+2x16=44 g/mol;
H2O :2-16=18 g/mol ;
CH4: 12+4 = 16 g/mol
1.n(C3H8)=Masse (g) / masse molaire =15 000 / 44 = 341 mol propane donc : d'après les coefficients de l'équation bilan
4x341 = 1364 moles d'eau ou 1364x18 = 24,5 kg eau
3x341 = 1023 moles CO2ou1023x44 = 45 kg
2. n(CH4)=volume (L) / volume molaire des gaz(L/mol)=1500 x1000 / 24 = 62500 mol méthane
2.1. Masse de méthane brulée:62500x16 = 1000 kg.
2.2 Volume CO2: 62500x44 = 2750 kg.
Volume Eau: : 2x62500 = 125 000 mol soit 125000x18 =2250 kg eau
2.4 Volume de dioxygène:
n(O2)=2x62500=125000 mol de O2
Volume (L) = Qté de matière (mol) * volume molaire des gaz (L/mol) : 125000x24 = 3 000 m³
Volume d'air : 3000x5 = 15 000 m3
Avez-vous un exercice à proposer ?Cliquez-ici
Merci de votre visite