CORRIGES
EXERCICE I:
1.Especes en solution: ![]() ; Cu2+;
H3O+; H2O
; Cu2+;
H3O+; H2O
Oxydations possibles à l’anode :
![]() (1)
(1)
3H2O →1/2O2 +2H3O+ +2e (2)
Réductions possibles à la cathode:
2H3O+ +2e→H2 +2H2O (3)
Cu→Cu2+ +2e (4)
Les réactions devant se produire sont: (2) et (4)
2-La fem minimum à appliquer est E(O2/H2O) - E(Cu2+/Cu) =1,23-0,34=0,89 V.
EXERCICE II:
1-Réductions possibles à la cathode
2H2O + 2e → H2+2HO- (a)
Na+ + e → Na (b)
Oxydations possibles à l’anode:
3H2O → 1/2O2 +2H3O+ +2e (c)
2Cl- → Cl2 +2e (d)
Au vu des potentiels de ces couples ce sont les réactions (a) et (c) qui devraient se produire.
2-Ce résultat expérimental n’est pas en accord avec les prévisions. En effet, c’est la réaction(d) au lieu de la (c) qui se produit.
3-Equation globale de la réaction:
2H2O + 2(Na+ + Cl-) → H2+Cl2 +2(Na + HO-)
2mol 1mol
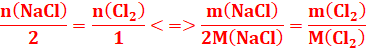
![]()
EXERCICE III:
1-Pour protéger la coque d’un bateau en fer, on doit utiliser un des métaux plus réducteurs que le fer, soit le zinc, soit le magnésium.
2-Cette diminution s’explique par le fait que le zinc étant plus réducteur que le fer, va s’oxyder en présence des agents corrosifs:
Zn→Zn2+ +2e
Calcul de la masse de er qui aurait été oxydée en l’absence du Zinc:
Fe→Fe2+ +2e
Il y a conservation de la quantité d’électricité, on constate que pour l’oxydation d’une mole de zinc ou une mole de fer, il y a libération de deux moles d’électrons, soit:
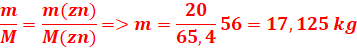
EXERCICE IV:
Dans les deux cas si la couche protectrice du Zn ou de Ni est sans fissures, la protection du fer est assurée, En revanche s’il y a fissure sur la couche, on assistera à:
-Comme E(Fe2+/Fe) > E(Zn2+/Zn) donc le réducteur le plus fort est le zinc, le zinc va s’oxyder et il y aura toujours protection du fer.
-Comme E(Ni2+/Ni)> E(Fe2+/Fe) donc le fer est plus réducteur plus fort que le nickel, il y aura une accélération de l’oxydation du fer.
EXERCICE V:
1.Il s’agit d’une protection électrochimique ou le métal plus réducteur Mg a s’oxyder:
Mg → Mg2+ +2e
2.Equation bilan de la réaction:
O2 +4H3O+ +4e→6H2O
Mg→Mg2+ + 2e
Bilan:
O2 +4H3O+ + Mg → 6H2O + 2Mg2+
1mol 2mol
Calcul de la masse de dioxygène:
![]()