CORRIGES
EXERCICE I:
1- Demi-équations des réactions d’oxydation des ions Fe2+ et de réduction des ions MnO-4 en milieu acide.
Fe2+ "Fe3+ + è
MnO-4 + 8H3O+ + 5è → Mn2+ + 12H2O
Équation bilan de la réaction entre les ions Fe2+ et MnO-4.
MnO-4 + 8H3O+ + 5Fe2+ → Mn2+ + 12H2O + 5Fe3+
2-Volume d’une solution de KMnO4
![]()
1-Equation bilan du dosage.
MnO-4 + 8H3O+ + 5Fe2+ → Mn2+ + 12H2O + 5Fe3+
2- Concentration de la solution réductrice en ions Fe2+
![]()
Masse m de sulfate de fer II .
m=Mxn(Fe2SO4)=MCrVr=x152x0,386x005=2,93 g
EXERCICE III:
1- Pour repérer l’équivalence de façon précise, il faut ajouter d‘empois d’amidon.
2- A l’équivalence,
CoVO = 2CrVr => C0 = CrV0/2V0=0,1x10/2x11,2=0,045 mol/l
EXERCICE IV :
1-
M=57+32+4x16+30=172 g/mol
n=m/M et c=n/V=m/MV =>m=cVM=0,1x500.10-3x182=9,1 g
-Il doit peser 9,1 g de FeSO4 ,2H2O et l’introduire dans une fiole jaugée de 500 ml
- ajouter environ 50 ml d’eau distillée dans la fiole et agiter.
-compléter ensuite avec l’eau distillée jusqu’au trait de jauge et agiter une dernière fois.
2-
![]()
La solution a été bien préparée.
EXERCICE V :
1- Il
est question ici de proposer un mode opératoire du dosage effectué.
Schéma du dispositif expérimental :
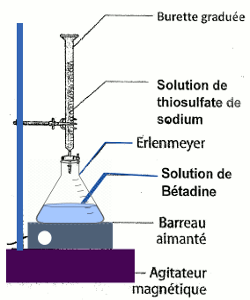
Protocole
de dosage :
• Remplir la burette avec la solution de thiosulfate de sodium ;
• Introduire 10 mL de la solution diluée de Bétadine dans L’erlenmeyer ou le
bécher et y ajouter quelques gouttes d’empois d’amidon ;
• Faire couler progressivement la solution de thiosulfate de sodium contenue
dans la burette ;
• L’équivalence est obtenue par la décoloration du mélange contenu dans le
bécher ou l’erlenmeyer.
Autre
Protocole à valider :
Verser progressivement la solution diluée de thiosulfate de sodium de la
burette dans le bécher ou l’erlenmeyer contenant l0 mL de solution diluée de
Bétadine.
A l’équivalence on observera une décoloration de la solution du ‘bécher ou de
l’erlenmeyer. (Passage du jaune-brun à l’incolore ou du bleu à l’incolore si on
a utilisé de l’empois d’amidon).
2- Il
est question de vérifier si la solution de Bétadine est encore utilisable.
Pour cela :
• Calculer la valeur deC1(I2)
• Déduire celle deC0(I2)
• Calculer la valeurP(I2)
• Vérifier siP(I2)est compris dans l’interva1le[8%−10%]
• Conclure.
• Equation-bilan support du dosage
2S2O2−3+I2→S4O2−6+2I−
Déterminons la concentration de la solution diluéeC1
A L’équivalence on a :
n(S2O2−3)/2=n(I2)/1;
C2V2/2=C1V1⇒C1=C2V2/2V1
C1=0,0405mol/ L
• Déterminons la concentrationC0(I2)
C0(I2)=10C1(I2)=0,405mol/L
• DéterminonsP(I2)
P(I2)=0,405×2×127×1001,03×1000=9,997%
P(I2)=9,997%≈10%
Conclusion:P(I2)étant compris dans l’intervalle[8%−10%].
La solution de Bétadine trouvée dans la boite à pharmacie est encore utilisable
EXERCICE VI:
Tâche
1 :
• Problème scientifique : description du protocole du dosage deSO2du
vin par les ions permanganate.
• Actions à mener :
1. Dessiner le dispositif expérimental du dosage ;
2. Décrire le mode opératoire du dosage.
• Résolution :
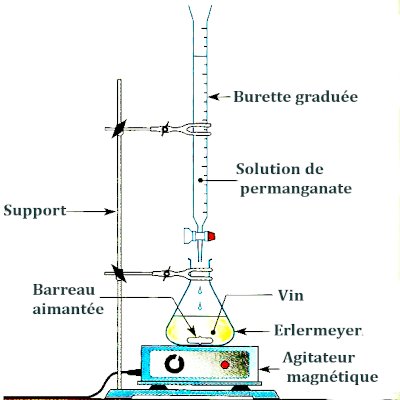
On
réalise le montage ci-dessus ;
• Prélever à l’aide d’une pipette 20 mL de vin acidifié (solution de dioxyde de
soufre) qu'on verse dans un erlenmeyer ou un bécher ;
• Remplir la burette graduée avec la solution de permanganate ;
• Laisser couler la solution de la burette mL par mL, puis goutte par goutte en
prenant soin d’agiter le mélange jusqu’à la persistance de la teinte violette
dans l’erlenmeyer (point d’équivalence).
• Relever la descente de burette qui correspond au volume à l’équivalence
(faire la moyenne après plusieurs essais).
Tâche
2 :
• Problème scientifique : détermination de la concentration enSO2du
vin-
• Actions à mener :
1. Exploiter l'équation-bilan support du dosage pour établir la relation entre
les quantités de matières deSO2et deMnO−4.
2. Exprimer et calculer la concentration en S02 du vin.
3. Comparer à la norme et conclure.
• Résolution :
D’après l’équation-bilan support du dosage on a, à l’équivalence :
2MnO−4
+5SO2+6H2O → 2Mn2++5SO2−4+4H3O+
n(Mn O−4)
=n(SO2)5⇒n(SO2)=5/2n(MnO−4)
[SO2]=5/2[MnO−4]Ve/Vvin=2,5x10-3x17,2/20
AN :[SO2]=2,15×10−3= 2,15mmol/L
• Comparaison et conclusion : 2,15 mmol/L < 6, 5mmol/L, alors le vin est
encore conforme à la législation