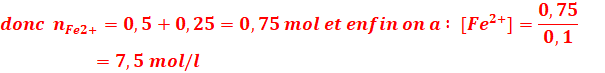CORRIGES
EXERCICE I::
a)
(x3) Cu→Cu2+ +2e
(x2) NO-3 + 4H3O+ + 3è+ ⇆ NO + 6H2O
3Cu+2NO-3 +8H3O+ ⇆3Cu2+ +2 NO+12 H2O
Espece oxydante: NO-3
Espece reductrice: Cu
b) ll y a absence d’ions H3O+ dans la solution.
EXERCICE II:
1- (x3) Cu→Cu2+ +2e
(x2) NO-3 + 4H3O+ + 3è+ ⇆ NO + 6H2O
3Cu+2NO-3 +8H3O+ ⇆3Cu2+ +2 NO+12 H2O
2- masse du cuivre
![]()
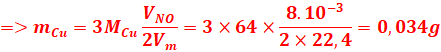
EXERCICE III:
1-
2-
2.1- MnO-4 /Mn2+ et Cl2/Cl-
2.2-
2Cl- → Cl2 +2è
MnO-4 + 8H3O+ + 5è ⇆ Mn2++ 12H2O
2.3- équation-bilan équilibrée de la réaction.
10Cl- +2MnO-4 + 16H3O+ ⇆ 5Cl2+2 Mn2+ + 24H2O
3-
3.1- ViCi=VfCf=>Vi= VfCf/Ci=1x2.10-2/0,5=0,02 l
3.2- Porter des gants et des lunettes de protection.
EXERCICE IV:
1-Concentration des ions Fe3+ et en ion a SO2-4 de la solution.
M=2x56+3(32+4x16)=400
n=10/400=0,025
c=n/V=0,025/0,1=0,25 mol/l
Fe2(SO4)3 → 2Fe2+ + 3SO2-4
![]()
![]()
![]()
![]()
2-’équation bilan de la réaction.
2Fe3+ + Fe → 3Fe2+
3-variations de la masse de Fer métallique lorsque tous les ions Fe2+ ont été réduits.
![]()
![]()
4-Calcul de la concentration en ion Fe2+
Les
ions Fe2+sont
issus de la réduction des ions ![]() :
: ![]()