CORRIGES
EXERCICE II:
1. HCOOH+H2O→HCOO- + H3O+
2.
2.1- HCOOH +HO- →HCOO- +H2O
2.2-A l’équivalence, nA=nB < =>CAVA=CBVBE =>VBE=CAVA/CB=0,1x20/0,25=8 ml.
2.3-Les ions HCOO- sont majoritaires or HCOO- est la base conjuguée de HCOOH => solution basique
2.4-Le BBT et l’hélianthine est conseillé pour un dosage acide faible-base forte.
2.5-
EXERCICE II:
a)
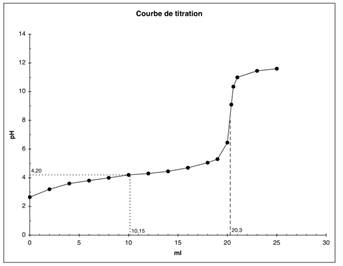
b) Le point d'équivalence est déterminé graphiquement : Véq = 20,3 mL.
On calcule ensuite la concentration de l'acide avec la formule CA ⋅ VA = CB⋅ VB : => CA = CB⋅ VB /VA = 0,1⋅ 0,0203 /0,020 = 0,1015 mol⋅ L−1
c) A la demi-titration, on a pH = pKa. La lecture graphique donne pKa = 4,2.
EXERCICE III:
1° a)
C2H3NH2 +H3O+ → C2H3NH3+ + H2O
b)
A l’équivalence, la réaction ci-dessus est terminée: on constate depuis la traduction de l’équation, qu’on a utilisé le même nombre nb moles de molécules C2H3NH2 et de moles na d’ions H3O+.
CaVaE = CbVb pour l’expérience I.
CaVa = CbVbE pour l’expérience II.
Par la méthode des tangentes, on trouve le point E représentant l’équivalence:
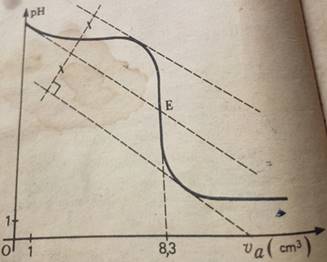
Expérience I: On verse progressivement la solution basique dans Va=10cm3 de solution acide. D’après la courbe I, l’équivalence est atteinte pour VbE=10 cm’
VaE=8,3 cm3; Ca=10-1mol/l;Vb=10cm3
CbI=CaVaE/Vb=10-1x8,3/10=8,3.10-2 mol/l
Expérience II: On verse progressivement la solution acide dans Vb=10cm3 de solution basique. D’après la courbe II, l’équivalence est atteinte pour VaE=8,3 cm’
VaE=10 cm3; Ca=10-1 mol/l; VbE=12 cm3
CbII=CaVa/VbE=10-1x10/12=8,33.10-2mol/l
On constate que ces valeurs sont égales a moins de 2% près, ce qui est compatible avec les difficultés d’appréciation des volumes.
2°
Entre le pH d’une solution de monoéthylamine et le pKa du couple, il existe la relation:
pH=pKA
+ ![]()
Quand [C2H5NH2]=[ C2H5NH3+].ce qui est le cas à la demi-équivalence, pH=pKA
Courbe I =>a la demi-équivalence Va=VbE/2 donc Va=4,15 cm3 et on lit le pH correspondant 10,8
ð pKA=10,8 pour le couple C2H5NH3+/C2H5NH2
EXERCICE IV:
1- Protocole permettant d’aboutir au point de demi-équivalence
Dosage pH-métrique d'une solution d'acide faible All par une base l'uneHO−
♦ Après avoir rincé la verrerie,
♦ Introduire un volume Va de la solution d'acide faible dans un bûcher ;
♦Introduire la solution de base forte dans la burette graduée jusqu'à la
graduation zéro (0);
♦Plonger les électrodes du pH-mètre préalablement étalonné dans le
bécher:
♦ Mettre en marche l’agitateur magnétique ;
♦ Verser progressivement la solution de base forte dans le bécher ;
♦ Noter chaque fois la valeur du pH indiquée par le pH-mètre
correspondant au volume de base versé ;
A l'aide des résultats obtenus, tracer la courbepH=f(Vb);
♦ Déterminer le volume à l'équivalenceVbE; par la
méthode des tangentes parallèles ;
♦ Calculer le volume a la demi-équivalenceVb(12eq)=Vbeq2de
base à verser
♦ Reprendre le dosage en laissant couler un volumeVbeq2de la
solution de base forte dans le bécher contenant le volume Va initial de la
solution d'acide faible et lire le pH correspondant au mélange obtenu.
Dispositif expérimental.
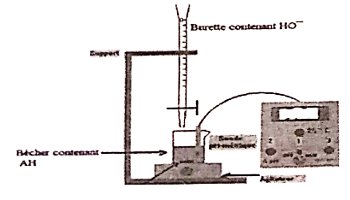 2- Le problème posé :
Préparation d'une solution tampon depH=9,2
2- Le problème posé :
Préparation d'une solution tampon depH=9,2
pH=pKa+log[NH3][NH+4]=9,2=pKa(NH+4/NH3)
1| faut que[NH+4]=[NH3]pour
avoirpH=pKa.
N'ayant pas les ionsNH+4en solution, il faut
les produire en faisant réagirNH3avecH3O+.
Suivant l'équation de la réaction :
NH3+H3O+→NH+4+H2O
Réactif à choisir : Ammoniac et acide chlorhydrique.
Il faut doser l’ammoniac par l'acide chlorhydrique jusqu'à la demi-
équivalence1,5 pt
Calcul des volumes l'acide et de base à prélever
ð 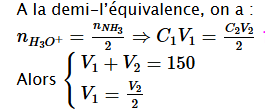
Car, ces solutions ont une même concentration
On trouveV1=50mL etV2=100mL1
Pour répondre au besoin de la commande, ATEBA doit :
Réaliser dans un bécher un mélange 50 mL de solution d’acide chlorhydrique et
100 mL de solution d'ammoniac.
Ou bien il doit introduire 100 mL de solution d’ammoniac dans un bécher puis à
l’aide d'une burette laisser couler 50 mL de solution d'acide chlorhydrique.
Le mode de préparation de la solution tampon commandé peut être acheminé au
principal du collège Bilingue les COMPÉTENTS
EXERCICE VI:
Examinons
si Eric a relevé son défi. Pour cela on va :
•Déterminer le réactif limitant
• Exploiter l'équation bilan de la réaction ;
• Déterminer la masse d'aspirine synthétisé ;
• Comparer à la masse escomptée
• Conclure
1) Détermination du réactif limitant
soit nas la quantité de matière de l’aspirine et nac,
celle de l’anhydride éthanoïque.
![]()
![]()
![]()
Déterminons la masse d’aspirine synthétisée
Soit: m3(obt) la masse d’aspirine obtenue et m3(att) celle d’aspirine attendue théoriquement.
m1 la masse d’acide salicylique et M1 la masse molaire d’acide salicylique
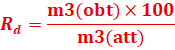
D’après l’équation-bilan:
![]()
Conclusion :88,7g≺100gdonc Erie n'a pas relevé son défi.
2 : Vérification de la masse d'aspirine sur l'étiquette.
Démarche
:
• Écrire la relation à l'équivalence
• Déterminer ln concentrationCade la solution d’aspirine
;
• Déterminer la masse d'aspirine contenu dans la solution préparée ;
• Comparer à la masse de l'étiquette puis conclure.
Relation à l'équivalence
Il s'agit du dosage de l'aspirine contenant une fonction acide carboxylique par
une monobase forte (hydroxyde de sodium)
Équation bilan de la réaction du dosage :

Détermination de la concentration Ca de la solution d’aspirine
![]()
CA=11x10-3 mol/l
Détermination de la masse d’aspirine contenue dans la solution préparée (V=500 ml)
![]()
Conclusion : La masse sur le sachet d’aspirine est conforme
EXERCICES VII :
I.
Protocole :
• Introduire un volumeVB= 20 mL de la solution de
vinaigre dans un bécher :
• Introduire la solution d’hydroxyde de sodium dans la burette
• Plonger les électrodes de pH-mètre préalablement étalonné dans le bécher
• Mettre en marche l’agitateur magnétique;
• Verser progressivement la solution de base forte dans le bécher ;
• Noter chaque fois la valeur du pH indiquée par le pH-mètre correspondant au
volume de base versé et cela permettra de tracer la courbepH=f(VB).
• Schéma du dispositif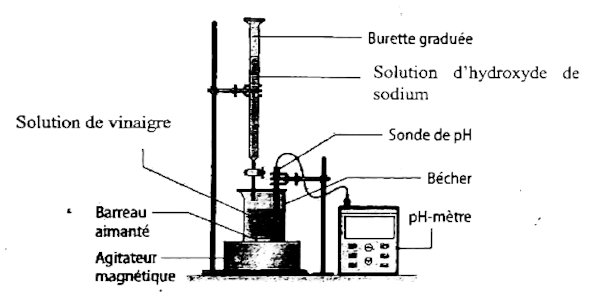
2- Vérification de la conformité du degré du vinaigre.
Actions à mener :
Écrire l’équation-bilan support du dosage ;
Déterminer graphiquementVBE;
Déterminer la concentration d`acide contenu dans l’échantillon dosé ;
En déduire le degré du vinaigre ou pourcentage massique d`acide éthanoïque ;
Comparer à celui porté sur l’étiquette
Conclure.
Résolution
CH3−COOH+OH−→CH3−COO−+H2O
Graphiquement on trouveVBE=26,8mL
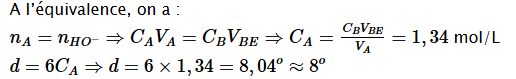
Conclusion : L’indication portée sur l’étiquette est conforme.