CORRIGES
EXERCICE I:
1.Le trouble de l’eau de chaux indique la formation de CO₂.
→ Conclusion : La substance contient du carbone, car sa combustion a produit du dioxyde de carbone, qui trouble l’eau de chaux.
2.
- Le noircissement est dû au carbone libéré : → présence de carbone.
- La buée montre la présence de vapeur d’eau : → présence d’hydrogène (dans H₂O).
Donc, le sucre contient carbone et hydrogène.
3.
Réaction chimique : C + O₂ → CO₂
L’eau de chaux se trouble → présence de CO₂
Conclusion : L’échantillon contient du carbone.
EXERCICE II:
1 :
a- Noircissement (carbone libéré), gouttelettes sur les parois (eau).
b-Le glucose contient du carbone (car charbon noir formé) et de l’hydrogène (eau formée).
c-Faire passer les gaz dans de l’eau de chaux → elle se trouble si CO₂ est présent.
2.
L’eau de chaux détecte le CO₂.
Le trouble observé prouve que du dioxyde de carbone a été formé, donc que la substance contenait du carbone.
3 .
- Le sucre est une substance organique, donc contient carbone et hydrogène → noircissement (carbone), buée (H₂O).
- Le sel est un composé minéral, il ne contient pas de carbone → aucune transformation visible.
→ Seules les substances organiques contiennent du carbone détectable par chauffage.
EXERCICE III :
1.Mise en évidence de l’azote dans une protéine
a- Le papier pH devient bleu → présence d’un gaz basique.
b- Le gaz formé est l’ammoniac (NH₃), à l’odeur piquante.
c-L’ammoniac vient de l’azote contenu dans la gélatine.
→ La gélatine contient donc de l’azote
2.Test de l’azote dans un engrais azoté
a-Gaz : ammoniac (NH₃).
b-L’acide réagit avec le NH₃ pour former des fumes blanches (chlorure d’ammonium).
c-L’engrais contient bien de l’azote, car l’ammoniac en est issu.
3.Détection d’azote dans la laine
a- Odeur piquante d’ammoniac.
b-Le papier devient bleu → présence d’un gaz basique.
c-Conclusion : la laine contient de l’azote
EXERCICE IV :
1 .
a- n(CO₂) = 1,100 / 44 = 0,025 mol
Chaque mole de CO₂ contient 1 mol de C ⇒ n(C) = 0,025 mol
m(C) = n × M = 0,025 × 12 = 0,300 g de carbone
![]() =60%
=60%
// autre méthode
![]() =
=![]() =0,3g
=0,3g
![]() =
=![]() =60%
=60%
2 : n(CO2)=1,320/44=0,03 mol
n(C)=0,03 mol
m(C)=0,03x12=0,36 g
%C=(0,36/0,800)x100=45%
3.
![]()
![]()
![]()
![]()
→ Formule brute = C₂H₆O
EXERCICE V :
1. Déterminer les masses de C et H
a. Masse de carbone dans CO₂ :
CO₂ contient 12 g de C pour 44 g de CO₂
→ m(C) = (12/44) × 0,880 g ≈ 0,24 g
b. Masse d’hydrogène dans H₂O :
H₂O contient 2 g de H pour 18 g de H₂O
→ m(H) = (2/18) × 0,360 g ≈ 0,04 g
- Masse de l'élément manquant (Oxygène)
m(O) = masse du composé – m(C) – m(H)
m(O) = 0,400 – 0,24 – 0,04 = 0,12 g
-Déterminer les moles de C, H et O
- n(C) = 0,24 / 12 = 0,020 mol
- n(H) = 0,04 / 1 = 0,040 mol
- n(O) = 0,12 / 16 = 0,0075 mol
-Déterminer les rapports simples
Divisons par le plus petit : 0,0075
- C : 0,020 / 0,0075 ≈ 2,67
- H : 0,040 / 0,0075 ≈ 5,33
- O : 0,0075 / 0,0075 = 1
→ On multiplie tout par 3 pour obtenir des entiers :
- C ≈ 8
- H ≈ 16
- O = 3
Formule brute : C₈H₁₆O₃
2 .
1. C : 0,220 / 44 = 0,005 mol
2. H : 0,090 / 18 = 0,005 mol × 2 = 0,010 mol
3. N : 0,035 / 28 = 0,00125 mol
Rapport :
- C : 0,005 / 0,00125 = 4
- H : 0,010 / 0,00125 = 8
- N : 0,00125 / 0,00125 = 1
→ Formule brute : C₄H₈N
EXERCICE VI:
1. ![]()
![]()
![]()
2.
![]()
![]()
![]()
3.Soit CxHyOz la formule brute de ce corps
%O=100-(52,2+13) =34,8%
![]()
![]()
![]()
La formule est C2H6O
EXERCICE VII:
1.Déterminons le pourcentage de carbone, de l’hydrogène et d’azote contenus dans le composé étudié.
![]()
![]() =
=![]() =15,56%
=15,56%
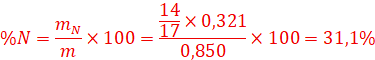
![]()
2. formule brute:CxHyNz
M=29d=29x1,55=44,95
![]()
![]()
![]()
Formule brute:C2H7N
EXERCICES VIII:
1.Commençons par déterminer la quantité de matière de diazote (N₂) à l'aide de l'équation des gaz parfaits :
Données :
- V(N₂) = 115 cm³ = 0,000115 m³
- T = 25°C = 298 K
- P = 930 hPa = 93 000 Pa
- R = 8,31 J·mol⁻¹·K⁻¹
Équation des gaz parfaits :
PV = nRT → donc n = PV / RT
Remplaçons les valeurs :
n = (93 000 × 0,000115) / (8,31 × 298)
n ≈ (10,695) / (2477,38) ≈ 0,004316 mol
2. Masse molaire de la substance :
n(N) = 0,00864 mol (car 1 mol de N₂ = 2 mol de N)
![]()
![]()
1. Formule brute: CxHyNz
![]()
![]()
![]()
![]()
![]()
Formule brute:CH5N